Odisha State Board BSE Odisha 9th Class Physical Science Notes Chapter 3 ପରମାଣୁ ଓ ଅଣୁ will enable students to study smartly.
BSE Odisha Class 9 Physical Science Notes Chapter 3 ପରମାଣୁ ଓ ଅଣୁ
→ ଉପକ୍ରମ (Introduction):
(i) ପ୍ରାଚୀନ ଭାରତର ଦାର୍ଶନିକ ମହର୍ଷି କଣାଦ (400 BC)ଙ୍କ ପରିକଳ୍ପନା ଅନୁଯାୟୀ, ପଦାର୍ଥକୁ ବିଭାଜନ କରି ଚାଲିଲେ କ୍ଷୁଦ୍ରରୁ କ୍ଷୁଦ୍ର କଣିକା ମିଳିବ । କିନ୍ତୁ ଶେଷରେ ଏପରି ଏକ ଅବସ୍ଥା ଆସିବ ଯେତେବେଳେ କ୍ଷୁଦ୍ର କଣିକାକୁ ଆଉ ବିଭାଜନ କରି ହେବ ନାହିଁ । ଏହି କ୍ଷୁଦ୍ରତମ କଣିକାକୁ ସେ ପରମାଣୁ ନାମ କରିଥିଲେ।
(ii) ଭାରତୀୟ ଦାର୍ଶନିକ ପାକୁଧା କାତ୍ୟାୟନଙ୍କ ମତରେ କଣିକାଗୁଡ଼ିକ ସାଧାରଣତଃ ସମ୍ମିଳିତ ଭାବରେ ରହିଥା’ନ୍ତି ଏବଂ ଅନେକ ପ୍ରକାର ପଦାର୍ଥ ଗଠନ କରିଥା’ନ୍ତି ।
(iii) ଗ୍ରୀକ୍ ଦାର୍ଶନିକ ଲିଉସିପ୍ଟସ୍ ଏବଂ ଡିମୋକ୍ରିଟସ୍କଙ୍କ ମତରେ, ପଦାର୍ଥଗୁଡ଼ିକ କ୍ଷୁଦ୍ର ଏବଂ ଅବିଭାଜ୍ୟ କଣିକାଗୁଡ଼ିକୁ ନେଇ ଗଠିତ ହୋଇଥାଏ । ଡିମୋକ୍ରିଟିସ୍ ଏହି କ୍ଷୁଦ୍ର କଣିକାର ନାମ ଆଟମ୍ ଦେଇଥିଲେ । ଗ୍ରୀକ୍ ଭାଷାରେ ଆଟମ୍ର ଅର୍ଥ ‘ଅବିଭାଜ୍ୟ’ ।
![]()
→ ରାସାୟନିକ ସଂଯୋଗର ନିୟମ (Laws of Chemical Combination) :
(i) ଅଷ୍ଟାଦଶ ଶତାବ୍ଦୀର ଶେଷ ଭାଗରେ ବୈଜ୍ଞାନିକ ଏ. ଏଲ୍. ଲାଭଇସିଅର (1774) ବସ୍ତୁତ୍ଵ ସଂରକ୍ଷଣ ନିୟମ ପ୍ରତିପାଦନ କରି ରସାୟନ ବିଜ୍ଞାନର ଭିଭି ସ୍ଥାପନ କରିଥିଲେ ।
(ii) ବୈଜ୍ଞାନିକ ଜେ. ଏଲ୍. ପ୍ରାଉଷ୍ଟ (1797) ରାସାୟନିକ ସଂଯୋଗର ସ୍ଥିରାନୁପାତ ନିୟମ ପ୍ରତିପାଦନ କରିଥିଲେ ।
→ ମାସର ସଂରକ୍ଷଣ ନିୟମ | (Law of Conservation of Mass):
ଏକ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମୟରେ ବସ୍ତତ୍ଵର ସୃଷ୍ଟି ହୁଏ ନାହିଁ କିମ୍ବା ବିନାଶ ହୁଏ ନାହିଁ, କେବଳ ସଂରକ୍ଷିତ ଥାଏ । ଏହାକୁ ବସ୍ତୁତ୍ଵ ସଂରକ୍ଷଣ ନିୟମ କୁହାଯାଏ । ଅର୍ଥାତ୍, ଯେତେବେଳେ ଏକ ରାସାୟନିକ ପରିବର୍ତ୍ତନ ବା 2g ହାଇଡ୍ରୋଜେନ 71g କ୍ଲୋରିନ ସହ ପ୍ରତିକ୍ରିୟା କରି 73g ହାଇଡ୍ରୋଜେନ କ୍ଲୋରାଇଡ଼ ଉତ୍ପନ୍ନ ହୁଏ । ସହ ସମାନ ଥାଏ ।
ଉଦାହରଣ :
2g ହାଇଡ୍ରୋଜେନ 71g କ୍ଲୋରିନ ସହ ପ୍ରତିକ୍ରିୟା କରି 73g ହାଇଡ୍ରୋଜେନ କ୍ଲୋରାଇଡ଼ ଉତ୍ପନ୍ନ ହୁଏ ।
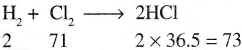
→ ସ୍ଥିରାନୁପାତ ନିୟମ (Law of Constant Proportions):
ଏକ ରାସାୟନିକ ଯୌଗିକରେ ମୌଳିକଗୁଡ଼ିକ ସର୍ବଦା ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ବସ୍ତୁତ୍ଵ ଅନୁପାତରେ ରହିଥାଏ । ଅର୍ଥାତ୍ କୌଣସି ଏକ ଯୌଗିକ ପଦାର୍ଥ ଯେପରି ପ୍ରସ୍ତୁତ ହେଉ ନା କାହିଁକି କିମ୍ବା ଯେକୌଣସି ଉତ୍ସରୁ ମିଳିଥାଉ, ସେଥୁରେ ସମାନ ମୌଳିକଗୁଡ଼ିକ ସର୍ବଦା ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ବସ୍ତୁତ୍ଵ ଅନୁପାତରେ ସଂଯୁକ୍ତ ହେବାଦ୍ଵାରା ତାହା ସୃଷ୍ଟି ହୋଇଥାଏ ।
![]()
ଉଦାହରଣ :
(i) କୂଅ, ପୋଖରୀ, ନଦୀ, ସମୁଦ୍ର ଆଦି ଜଳକୁ ସଂଗ୍ରହ କଲେ ମଧ୍ୟ ଜଳରେ ସର୍ବଦା ହାଇଡ୍ରୋଜେନ୍ ଓ ଅକ୍ ସି ଜେନ୍ 1 : 8 ବସ୍ତୁତ୍ଵ ଅନୁ ପାତରେ ସଂଯୁକ୍ତ ହୋଇଥାଏ । 9 ଗ୍ରାମ୍ ଜଳକୁ ବିଘଟନ (decompose) କଲେ ସର୍ବଦା 1 ଗ୍ରାମ୍ ହାଇଡ୍ରୋଜେନ୍ ଏବଂ 8 ଗ୍ରାମ୍ ଅକ୍ସିଜେନ୍ ମିଳେ ।
(ii) imf କାର୍ବନ ଓ ଅକ୍ସିଜେନ୍ର ବସ୍ତୁତ୍ଵର ଅନୁପାତ ସର୍ବଦା 3 : 8 ହେବ ।
→ ଡାଲ୍ନ୍ଙ୍କ ପରମାଣୁ ତତ୍ତ୍ବ (Dalton’s Atomic Theory):
ବୈଜ୍ଞାନିକ ଜନ୍ ଡାଲ୍ଟନ୍ 1808 ମସିହାରେ ପଦାର୍ଥର ଗଠନ ସମ୍ବନ୍ଧରେ ଏକ ନୂତନ ତତ୍ତ୍ଵ ଉପସ୍ଥାପନ କରିଥିଲେ । ଏହାକୁ ଡାଲ୍ନ୍ଙ୍କ ପରମାଣୁ ତତ୍ଵ କୁହାଯାଏ । ଏହି ପରମାଣୁ ତତ୍ତ୍ଵର ସ୍ଵୀକାରଗୁଡ଼ିକ ହେଲ୍।”
(i) ପଦାର୍ଥ ଅନେକଗୁଡ଼ିଏ ଅତି କ୍ଷୁଦ୍ର କଣିକାଦ୍ଵାରା ଗଠିତ । ସେହି କଣିକାକୁ ପରମାଣୁ କୁହାଯାଏ ।
(ii) ପରମାଣୁଗୁଡ଼ିକ ଅବିଭାଜ୍ୟ କଣିକା । ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଏହାକୁ ସୃଷ୍ଟି କରାଯାଇ ପାରିବ ନାହିଁ କିମ୍ବା ବିନାଶ କରାଯାଇ ପାରିବ ନାହିଁ ।
(iii) କୌଣସି ଏକ ମୌଳିକର ପରମାଣୁଗୁଡ଼ିକର ବସ୍ତୁତ୍ଵ ଓ ରାସାୟନିକ ଧର୍ମ ସମାନ ।
(iv) ବିଭିନ୍ନ ମୌଳିକର ପରମାଣୁଗୁଡ଼ିକର ବସ୍ତୁତ୍ଵ ଓ ରାସାୟନିକ ଧର୍ମ ଭିନ୍ନ ହୋଇଥାଏ ।
(v) ବିଭିନ୍ନ ମୌଳିକର ପରମାଣୁଗୁଡ଼ିକ ଛୋଟ ପୂଣ୍ଣ (small whole numbers) ପୂର୍ଣ୍ଣ ସଂଖ୍ୟା ଅନୁ ପାତରେ ସଂଯୁକ୍ତ ହୋଇ ଯୌଗିକ ସୃଷ୍ଟି କରନ୍ତି ।
![]()
ବିଜ୍ଞାନର ଅଗ୍ରଗତି ଯୋଗୁଁ ଡାଲ୍ନ୍ଙ୍କ ପରମାଣୁ ତତ୍ତ୍ଵ ସଂଶୋଧୃତ ହୋଇଛି । ପରମାଣୁକୁ ବିଭାଜନ କରି ହେଲାଣି । ପରମାଣୁ ମଧ୍ୟରେ ଏହାଠାରୁ କ୍ଷୁଦ୍ରତର ଏକାଧ୍ଵକ ଅବପରମାଣୁ (subatomic) କଣିକାମାନ ରହିଛି ।
→ ପରମାଣୁ (Atom):
(i) ପ୍ରତ୍ୟେକ ପଦାର୍ଥ ବହୁସଂଖ୍ୟକ ଛୋଟ ଛୋଟ ପରମାଣୁ ଦ୍ଵାରା ଗଠିତ ହୋଇଥାଏ ।
(ii) ପରମାଣୁକୁ ଖାଲି ଆଖୁରେ ଦେଖୁ ନ ପାରିଲେ ମଧ୍ୟ, ଆଧୁନିକ ବୈଷୟିକ ଜ୍ଞାନଦ୍ଵାରା ଏହାର ସ୍ଥିତି ପ୍ରମାଣିତ ହୋଇପାରିଛି ।
ବିଭିନ୍ନ ମୌଳିକର ପରମାଣୁମାନଙ୍କର ପ୍ରତୀକ :
ମୌଳିକର ସଂପୂର୍ଣ୍ଣ ନାମ ପରିବର୍ତ୍ତେ ବ୍ୟବହୃତ ହେଉଥିବା ସଂକ୍ଷିପ୍ତ ନାମକୁ ପ୍ରତୀକ (symbol) କୁହାଯାଏ ।
(i) ମୌଳିକର ପ୍ରତୀକକୁ ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ଅର୍ଥରେ ବ୍ୟବହାର କରିବାରେ ଡାଲ୍ଟ ଟନ୍ ହେଉଛନ୍ତି ପ୍ରଥମ ବୈଜ୍ଞାନିକ ।
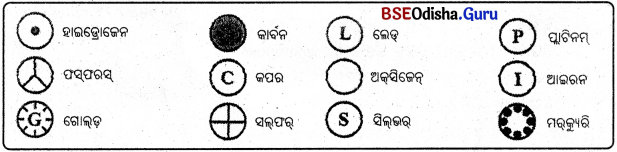
(iii) ବୈଜ୍ଞାନିକ ବର୍ଜିଲିୟସ୍କଙ୍କ ମତରେ ମୌଳିକ ନାମର ଗୋଟିଏ କିମ୍ବା ଦୁଇଟି ଅକ୍ଷରକୁ ନେଇ ସେହି ମୌଳିକର ପ୍ରତୀକ ଲେଖାଯାଇପାରେ ।
(iv) ବର୍ତ୍ତମାନ ଆନ୍ତର୍ଜାତିକ ବିଶୁଦ୍ଧ ଓ ପ୍ରୟୋଗାତ୍ମକ ରସାୟନ ସଂଘ (International Union of Pure and Applied Chemistry) ବା ଆଇୟୁପିଏସି (IUPAC) ମୌଳିକଗୁଡ଼ିକର ନାମ ଅନୁମୋଦନ କରନ୍ତି ।
(v) ଅଧିକାଂଶ ପ୍ରତୀକ ମୌଳିକର ଇଂରାଜୀ ନାମର ପ୍ରଥମ ଅକ୍ଷର କିମ୍ବା ପ୍ରଥମ ଦୁଇଟି ଅକ୍ଷର ନେଇ ଗଠିତ । ପ୍ରତୀକର ପ୍ରଥମ ଅକ୍ଷରଟି ସବୁବେଳେ ଇଂରାଜୀର ବଡ଼ ଅକ୍ଷର (capital letter) ଦ୍ଵିତୀୟଟି ଛୋଟ ଅକ୍ଷର (small letter) ଲେଖାଯାଏ ।
କେତେକ ମୌଳିକର ପ୍ରତୀକ, ଲାଟିନ୍ ନାମ, ଗ୍ରୀକ୍ ନାମ, ଇଂରାଜୀ ନାମ
ଲି ଖ୍ତ ଭାଷାର ନାମ
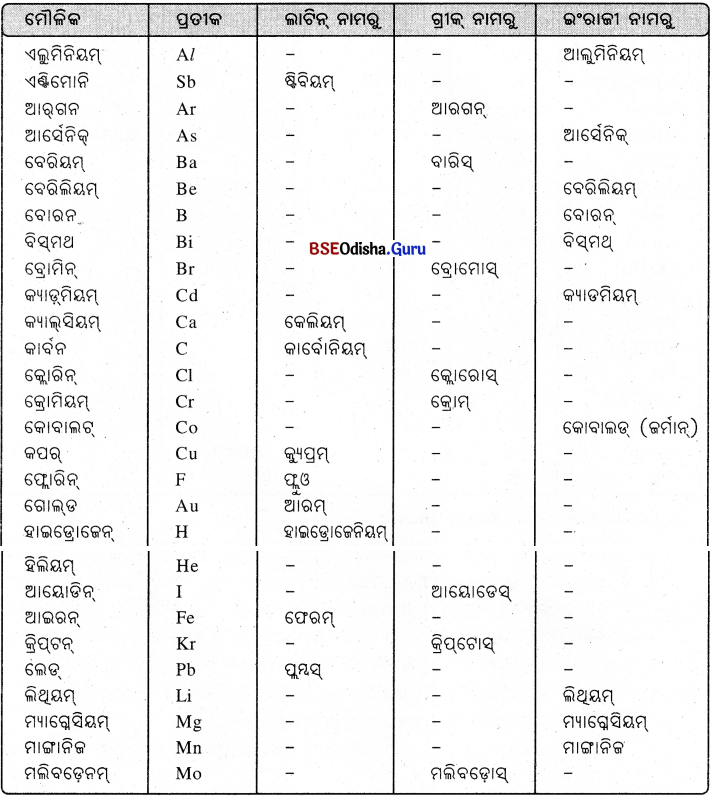
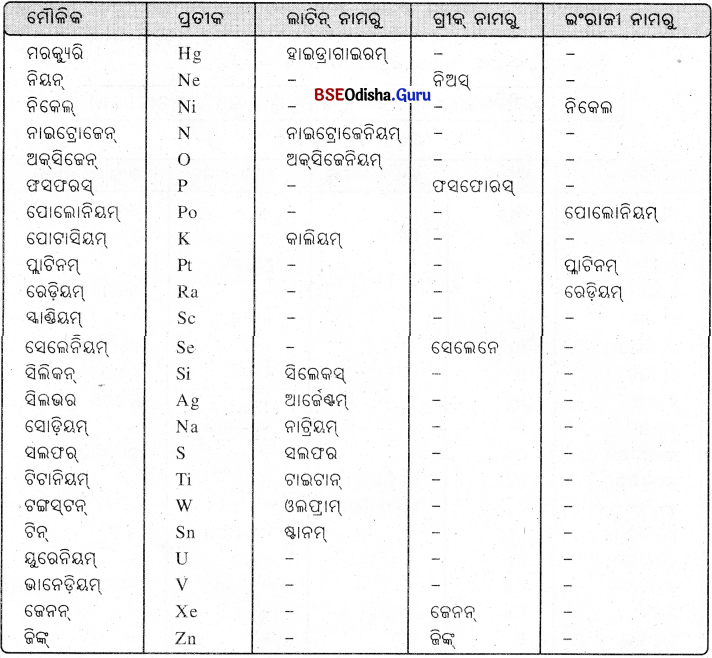
ପାରମାଣବିକ ବସ୍ତୁତ୍ୱ (Atomic Mass) :
(i) ପରମାଣୁର ବସ୍ତୁତ୍ଵ ଏତେ କମ୍ ଯେ, ଗୋଟିଏ ପରମାଣୁର ବସ୍ତୁତ୍ଵକୁ ସିଧାସଳଖ ମପାଯାଇ ପାରିବ ନାହିଁ । ତେଣୁ ବୈଜ୍ଞାନିକମାନେ ରାସାୟନିକ ସଂଯୋଗର ନିୟମ ଏବଂ ସୃଷ୍ଟି ହେଉଥିବା ଯୌଗିକକୁ ଉପଯୋଗ କରି ମୌଳିକର ତୁଳନାତ୍ମକ ବା ଆପେକ୍ଷିକ (relative) ବସ୍ତୁତ୍ଵ ନିର୍ଣ୍ଣୟ କରିଥିଲେ । ଏଥିପାଇଁ କୌଣସି ଏକ ପରମାଣୁର ବସ୍ତୁତ୍ଵକୁ ମାନକ ଏକକ (standard unit) ରୂପେ ନେଇ ଅନ୍ୟ ମୌଳିକର ପରମାଣୁର ବସ୍ତୁତ୍ଵ ନିର୍ଣ୍ଣୟ କରିବା ପାଇଁ ବୈଜ୍ଞାନିକମାନେ ନିଷ୍ପତ୍ତି ନେଇଥିଲେ ।
(ii) ପ୍ରଥମେ ବୈଜ୍ଞାନିକମାନେ ପ୍ରାକୃତିକ ଭାବରେ ମିଳୁଥିବା ଅକ୍ସିଜେନ୍ର ଗୋଟିଏ ପରମାଣୁର \(\frac {1}{16}\) ଭାଗ ବସ୍ତୁତ୍ଵକୁ ମାନକ ଏକକ ରୂପେ ନେଇଥିଲେ । କାରଣ –
(a) ଅନେକ ମୌଳିକ ସହିତ ଅକ୍ସିଜେନ୍ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରେ ଏବଂ ଯୌଗିକ ସୃଷ୍ଟି କରିପାରେ ।
(b) ଅଧିକାଂଶ ମୌଳିକର ପାରମାଣବିକ କୌଣସି ମୌଳିକର ପାରମାଣବିକ ବସ୍ତୁତ୍ୱ ବସ୍ତୁ ତ୍ଵ ଏହି ମାନ କ ଏ କ କ ନେ ବି। ଦ୍ଵାର। ପୂର୍ଣ୍ଣ ସଂଖ୍ୟା ହୋଇଥାଏ ।
(iii) 1961 ମସିହାରୁ ୯ ବା କାର୍ବନ−12 (ବା C-12) ସମାବୟବ (isotope) ର \(\frac {1}{12}\) ଭାଗ ବା ଅଂଶକୁ ମାନକ ଏକକ ରୂପେ ବିଶ୍ବବ୍ୟାପୀ ବ୍ୟବହାର କରାଗଲା
(iv) C ର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ 12 ଅଟେ । ଏହି ଏକକକୁ ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ ଏକକ (atomic mass unit) ବା ସଂକ୍ଷେପରେ amu କୁହାଯାଏ । ଏବେ ଏହି ଏକକକୁ ‘u’ (undefined mass) ଲେଖା ଯାଉଛି ।
(v) ଏକ C-12 ପରମାଣୁର \(\frac {1}{12}\) ଭାଗ ବସ୍ତୁତ୍ଵ ତୁଳନାରେ ଗୋଟିଏ ମୌଳିକର ପରମାଣୁର ବସ୍ତୁତ୍ଵ ହେଉଛି ସେହି ମୌଳିକର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ ।
(vi) ମୌଳିକର ପାରମାଣବିକ ବସ୍ତତ୍ଵ ଏକ ଆନୁ ପାତିକ ବା ତୁଳନାତ୍ମକ ମୂଲ୍ୟ ।
(vii) ପାରମାଣବିକ ବସ୍ତୁତ୍ଵକୁ ଗ୍ରାମ୍ରେ ପ୍ରକାଶ କଲେ ତାହାକୁ ଗ୍ରାମ୍ ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ କୁହାଯାଏ । କେତେକ ମୌଳିକର ପ୍ରତୀକ ଓ ଏହାର ପାରମାଣବିକ ବସ୍ତତ୍ଵ ହୋଇଥାଏ ।
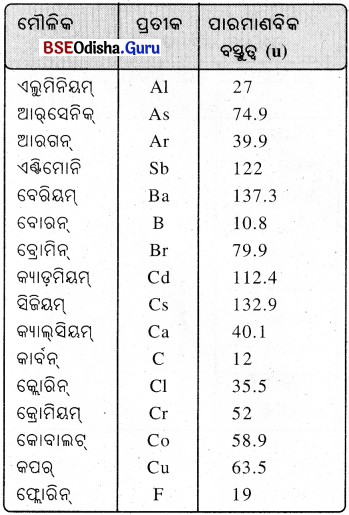
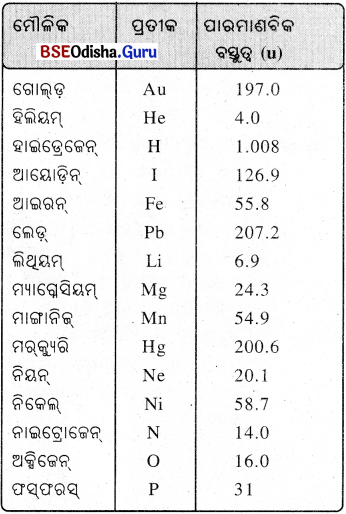
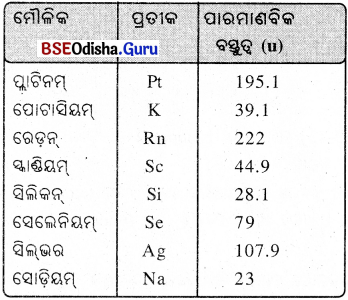
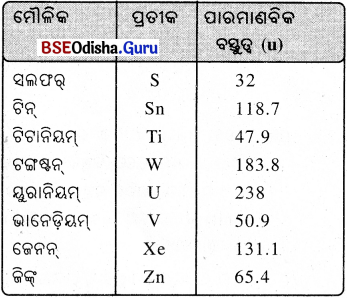
→ ଅଣୁ (Molecule) :
(i) ଅଣୁ ହେଉଛି ଏକ ମୌଳିକ କିମ୍ବା ଯୌଗିକର କ୍ଷୁଦ୍ରତମ କଣିକା ଯାହା ସ୍ଵାଧୀନ ଭାବରେ ରହିବାକୁ ଯୌଗିକର ସମସ୍ତ ଧର୍ମ ପ୍ରଦର୍ଶନ କରିଥାଏ ।
(ii) ସମର୍ଥ ଏବଂ ସେହି ମୌଳିକ କିମ୍ବା ଏକ ମୌଳିକର ଅଣୁ ଏକ ବା ଏକାଧିକ ସମଜାତୀୟ ପରମାଣୁକୁ ନେଇ ଗଠିତ ହୋଇଥାଏ ।
(iii) ଯୌଗିକର ଅଣୁ ସର୍ବଦା ଏକାଧିକ ଅସମଜାତୀୟ ପରମାଣୁକୁ ନେଇ ଗଠିତ ହୋଇଥାଏ ।
(iv) ଅଣୁ ମଧ୍ୟରେ ଥିବା ଏକାଧିକ ପରମାଣୁ ପରଷ୍ଟର ମଧ୍ୟରେ ରାସାୟନିକ ବନ୍ଧଦ୍ଵାରା ବାନ୍ଧି ହୋଇଥା’ନ୍ତି ।
![]()
→ ଉପାଦାନଗୁଡ଼ିକର ଅଣୁଗୁଡ଼ିକ (Molecules of Elements)
(i) ଏକ ମୌଳି କ ର ଅଣୁ ସମଜାତୀୟ ରମାଣୁକୁ ନେଇ ଗଠିତ ହୋଇଥାଏ ।
(ii) କେତେକ ମୌଳିକର ଅଣୁ ଗୋଟିଏ ପ ର ମ ଣୁ କୁ ନେ ଇ ହୋଇଥ୍ ବା ବେଳେ ଆଉ କେତେ କ ଦୁଇଟି କିମ୍ବା ତିନୋଟି କିମ୍ବା ଅନେକ ପରମାଣୁକୁ ନେଇ ଗଠିତ ହୋଇଥାଏ ।
(iii) ଅଣୁରେ ଥିବା ପରମାଣୁର ସଂଖ୍ୟାକୁ ତାହାର ପରମାଣୁକତା (atomicity) କୁହାଯାଏ ।
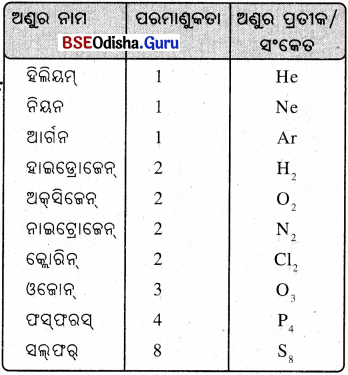
ଉଦାହରଣ :
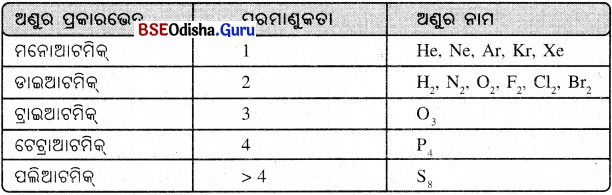
→ ଯୌଗିକର ଅଣୁ (Molecules of Compounds) :
(i) ବିଭିନ୍ନ ମୌଳିକର ପରମାଣୁଗୁଡ଼ିକ ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ଅନୁ ପାତରେ ଏକତ୍ର ମିଳିତ ହୋଇ ଯୌଗିକର ଅଣୁ ଗଠନ କରିଥା’ନ୍ତି ।
(ii) ଯୌଗିକର ଅଣୁ ଭିନ୍ନ ଜାତୀୟ ପରମାଣୁକୁ ନେଇ ଗଠିତ ହୋଇଥାଏ ।
ଉଦାହରଣ :
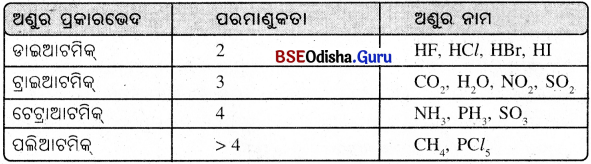
→ ଆୟନ (Ion) :
ଗୋଟିଏ ପରମାଣୁ ଇଲେକ୍ଟ୍ରମ୍ ଲାଭ କଲେ ବା ତ୍ୟାଗ କଲେ ଯେଉଁ ଚାର୍ଜିତ କଣିକା ସୃଷ୍ଟିହୁଏ, ଏହି ଚାର୍ଜଯୁକ୍ତ କଣିକାକୁ ଆୟନ କୁହାଯାଏ ।
(i) ଆୟନ ଯୁକ୍ତ ଚାର୍ଜ ବିଶିଷ୍ଟ ବା ବିଯୁକ୍ତ ଚାର୍ଜ ବିଶିଷ୍ଟ ହୋଇଥାଏ । NaCl → Na+ + Cl– ଯୁକ୍ତାତ୍ମକ ଚାର୍ଜିତ ଆୟନକୁ କ୍ୟାଟାୟନ (cation) ଏବଂ ବିଯୁକ୍ତାତ୍ମକ ଚାର୍ଜିତ ଆୟନକୁ ଆନାୟନ (anion) କୁହାଯାଏ ।
ଉଦାହରଣ : ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ ଯୌଗିକରେ ଥିବା ଚାର୍ଜଯୁକ୍ତ କଣିକାଗୁଡ଼ିକ ହେଉଛି ଯୁକ୍ତାତ୍ମକ ସୋଡ଼ିୟମ୍ ଆୟନ (Na+) ଓ ବିଯୁକ୍ତାତ୍ମକ କ୍ଲୋରାଇଡ୍ ଆୟନ (Cl–) ।
(ii) ଏକାଧିକ ପରମାଣୁ ଏକତ୍ର ହୋଇ ଚାର୍ଜ ବହନ କରୁଥିଲେ ସେଗୁଡ଼ିକୁ ପଲିଆଟମିକ୍ ଆୟନ (Polyatomic ion) କୁହାଯାଏ ।
(iii) ଜଳୀୟ ଦ୍ରବଣରେ ଆୟନ ସୃଷ୍ଟି ହେଲେ ଦ୍ରବଣଟି ବିଦ୍ୟୁତ୍ ସୁପରିବାହୀ ହୋଇଥାଏ । ଖାଇବା ଲୁଣରୁ ପ୍ରସ୍ତୁତ ଜଳୀୟ ଦ୍ରବଣରେ ଯୁକ୍ତାତ୍ମକ Na+ ଆୟନ ଓ ବିଯୁକ୍ତାତ୍ମକ C ଆୟନ ରହିଥାଏ । ତେଣୁ ଖାଇବା ଲୁଣର ଜଳୀୟ ଦ୍ରବଣ ବିଦ୍ୟୁତ୍ ସୁପରିବାହୀ ଅଟେ ।
(iv) ଚିନିର ଜଳୀୟ ଦ୍ରବଣରେ ଚିନି ଅଣୁର ବିୟୋଜନ (Dissociation) ହୁଏ ନାହିଁ ଏବଂ ଆୟନ ସୃଷ୍ଟି ହୁଏ ନାହିଁ । ତେଣୁ ଚିନିର ଜଳୀୟ ଦ୍ରବଣ ବିଦ୍ୟୁତ୍ ସୁପରିବାହୀ ନୁହେଁ ।
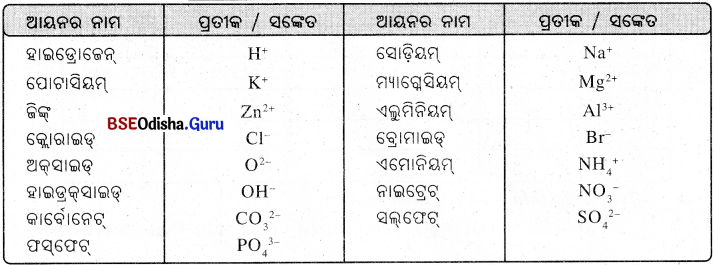
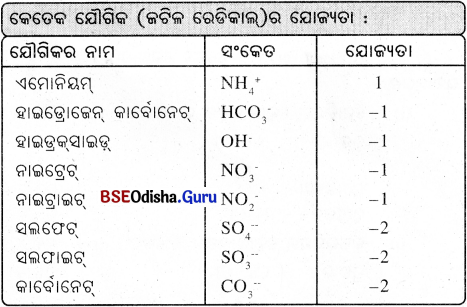
କେତୋଟି ଆନର ନାମ ଓ ପ୍ରତାକ/ସଙ୍କେତ:
→ ଯୋଗ୍ୟତା (Valency) :
ମୌଳିକର ସଂଯୋଜନ କ୍ଷମତାକୁ ଏହାର ଯୋଗ୍ୟତା (valency) କୁହାଯାଏ । ହାଇଡ୍ରୋଜେନ୍ ର ଯୋଗ୍ୟତାକୁ ଏକ ଧରି ଅଧିକାଂଶ ମୌଳିକର ଯୋଗ୍ୟତା ନିର୍ଣ୍ଣୟ କରାଯାଏ ।
ଉଦାହରଣ :
(a) ହାଇଡ୍ରୋକ୍ଲୋରିକ୍ ଏସିଡ୍ (HCl) ର ଗୋଟିଏ ଅଣୁରେ ଗୋଟିଏ କ୍ଲୋରିନ୍ ପରମାଣୁ ଗୋଟିଏ ହାଇଡ୍ରୋଜେନ୍ ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ କ୍ଲୋରିନ୍ର ଯୋଗ୍ୟତା ଏକ ଅଟେ ।
(b) ଜଳ (H2O) ଅଣୁରେ ଗୋଟିଏ ଅକ୍ସିଜେନ୍ ପରମାଣୁ ଦୁଇଟି ହାଇଡ୍ରୋଜେନ୍ ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ ଅକ୍ସିଜେନ୍ର ଯୋଗ୍ୟତା ଦୁଇ ଅଟେ ।
(c) ଏମୋନିଆ (NH3) ଅଣୁରେ ନାଇଟ୍ରୋଜେନ୍ ର ଗୋଟିଏ ପରମାଣୁ ହାଇଡ୍ରୋଜେନ୍ର ତିନୋଟି ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ ନାଇଟ୍ରୋଜେନ୍ର ଯୋଗ୍ୟତା ତିନି ଅଟେ ।
(d) ମିଥେନ୍ (CH4) ଅଣୁରେ କାର୍ବନର ଗୋଟିଏ ପରମାଣୁ ହାଇଡ୍ରୋଜେନ୍ର ଚାରୋଟି ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ କାର୍ବନର ଯୋଗ୍ୟତା ଚାରି ଅଟେ । ସମସ୍ତ ଯୌଗିକର ଉପାଦାନ ହାଇଡ୍ରୋଜେନ୍ ନୁହେଁ । ତେଣୁ ଅନ୍ୟ ମୌଳିକର ଯୋଗୁଁ ତାକୁ ଭିଭିକରି କେତେକ ମୌଳିକର ଯୋଗ୍ୟତା ନିର୍ଣ୍ଣୟ କରାଯାଇଛି ।
![]()
ଉଦାହରଣ :
(a) ସୋଡିୟମ୍ କ୍ଲୋରାଇଡ୍ (NaCl) ର ଗୋଟିଏ ଅଣୁରେ ଗୋଟିଏ ସୋଡ଼ିୟମ୍ ପରମାଣୁ ଗୋଟିଏ କ୍ଲୋରିନ୍ ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ ସୋଡ଼ିୟମ୍ର ଯୋଗ୍ୟତା ଏକ ଅଟେ ।
(b) ମ୍ୟାଗ୍ନେସିୟମ୍ କ୍ଲୋରାଇଡ୍ (MgCl2)ର ଗୋଟିଏ ଅଣୁରେ ଗୋଟିଏ ମ୍ୟାଗ୍ନେସିୟମ୍ ପରମାଣୁ ଦୁଇଟି କ୍ଲୋରିନ୍ ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହେଇଛି । ତେଣୁ ମ୍ୟାଗ୍ନେସିୟମ୍ର ଯୋଗ୍ୟତା ଦୁଇ ଅଟେ ।
(c) ଏଲୁମିନିୟମ୍ କ୍ଲୋରାଇଡ୍ (AlCl3)ର ଗୋଟିଏ ଅଣୁରେ ଗୋଟିଏ ଏଲୁମିନିୟମ୍ ପରମାଣୁ ତିନୋଟି କ୍ଲୋରିନ୍ ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ ଏଲୁମିନିୟମ୍ର ଯୋଗ୍ୟତା ତିନି ଅଟେ ।
(d) କାର୍ବନ ଟେଟ୍ରାକ୍ଲୋରାଇଡ୍ (CCl4)ର ଗୋଟିଏ ଅଣୁରେ ଗୋଟିଏ କାର୍ବନ ପରମାଣୁ ଚାରୋଟି କ୍ଲୋରିନ୍ ପରମାଣୁ ସହ ସଂଯୁକ୍ତ ହୋଇଛି । ତେଣୁ କାର୍ବନର ଯୋଗ୍ଯତା ଚାରି ଅଟେ ।
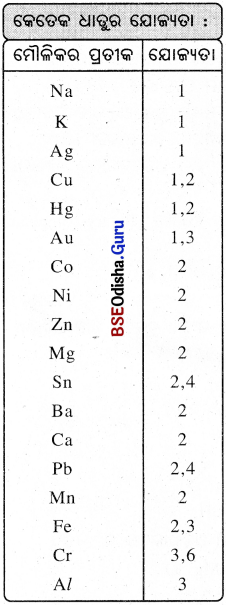
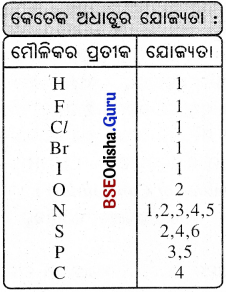
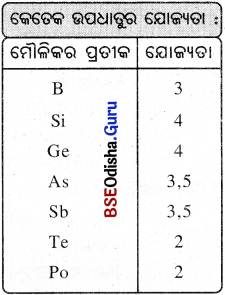
→ ଚଳ ଯୋଗ୍ୟତା (Variable Valency):
କେତେକ କ୍ଷେତ୍ରରେ ମୌଳିକର ଏକାଧ୍ଵକ ଯୋଗ୍ୟତା ଦେଖାଯାଏ । କୌଣସି ମୌଳିକର ଏକାଧିକ ଯୋଗ୍ୟତାକୁ ଚଳ ଯୋଗ୍ୟତା (Variable valency) କହନ୍ତି ।
ଉଦାହରଣ :
(i) ଫେରସ୍ ଅକ୍ସାଇଡ୍ (FeO) ରେ ଆଇରନ୍ର ଯୋଗ୍ୟତା 2 ଓ ଫେରିକ୍ ଅକ୍ସାଇଡ୍ (Fe,O)ରେ ଆଇରନ୍ର ଯୋଗ୍ୟତା 3 ଅଟେ ।
(ii) NÃO, NO, N,O, N,O, ଓ N,O, ଯୌଗିକଗୁଡ଼ିକରେ ନାଇଟ୍ରୋଜେନ୍ର ଯୋଗ୍ୟତା ଯଥାକ୍ରମେ 1, 2, 3, 4 ଓ 5 ଅଟେ ।
![]()
→ ରାସାୟନିକ ସୂତ୍ର। (Chemical Formula):
(i) ମୌଳିକ ବା ଯୌଗିକ ଅଣୁକୁ ସଂକ୍ଷେପରେ ଲେଖିବାକୁ ସଙ୍କେତ (Formula) କୁହାଯାଏ ।
(ii) ବିଭିନ୍ନ ଯୌଗିକର ରାସାୟନିକ ସଙ୍କେତ ଲେଖୁବାପାଇଁ ମୌଳିକର ପ୍ରତୀକ ଏବଂ ସଂଯୋଜନ କ୍ଷମତା (combining capacity) ସମ୍ବନ୍ଧରେ ଜାଣିବା ଆବଶ୍ୟକ ।
→ ରାସାୟନିକ ସଙ୍କେତ ଲେଖୁବାର ପ୍ରଣାଳୀ (Methods of writing Chemical Formula) :
ରାସାୟନିକ ସଙ୍କେତ ଲେଖିଲା ବେଳେ –
(i) ଆୟନର ଯୋଗ୍ୟତା କିମ୍ବା ଚାର୍ଜ ସମତୁଲ କରାଯାଏ ।
(ii) ଧାତୁ ଓ ଅଧାତୁରୁ ଗଠିତ ଯୌଗିକ ପାଇଁ ଧାତୁର ନାମ କିମ୍ବା ପ୍ରତୀକ ପ୍ରଥମେ ଲେଖାଯାଏ । ଉଦାହରଣ : ମ୍ୟାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ୍ – MgO, ପୋଟାସିୟମ୍ ବ୍ରୋମାଇଡ୍ – KBr
(iii) ପଲିଆଟମିକ୍ ଆୟନରୁ ସୃଷ୍ଟ ଯୌଗିକରେ ଆୟନକୁ ବନ୍ଧନୀ ମଧ୍ୟରେ ରଖ୍ ଅନୁ ପାତ ସୂଚାଉଥିବା ସଂଖ୍ୟାଟି ଲେଖାଯାଏ । ଯଦି ଏହି ସଂଖ୍ୟା ଏକ ହୋଇଥାଏ, ବନ୍ଧନୀର ଆବଶ୍ୟକତା ନଥାଏ । ଉଦାହରଣ – କ୍ୟାଲ୍ସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ – Ca(OH)2 ସୋଡ଼ିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ – NaOH
![]()
→ ଯୌଗିକର ସଂକେତ (Formulae of Compounds) :
(i) ଦୁଇଟି ପୃଥକ୍ ମୌଳିକରୁ ଗଠିତ ହୋଇଥିବା ଯୌଗିକକୁ ଦ୍ଵିଅଙ୍ଗୀ ଯୌଗିକ (Binary compound) କୁହାଯାଏ ।
(ii) ଆୟନର ଯୋଜ୍ୟତା ଆୟନ ଉପରେ ଦିଆଯାଇଥିବା ଚାର୍ଜରୁ ସୂଚନା ମିଳେ ।
(ii) କୌଣସି ଯୌଗିକ ଅଣୁର ଆଣବିକ ସଂକେତ ଲେଖିବାକୁ ହେଲେ ପ୍ରଥମେ ଏଥିରେ ଥିବା ମୌଳିଚ୍ଛୁଗୁଡ଼ିକର ପ୍ରତୀକକୁ ପାଖାପାଖୁ ଲେଖାଯାଏ । ମୌଳିକଗୁଡ଼ିକର ଯୋଗ୍ଯତା ସଂଖ୍ୟା ଦୁଇଟିର ସ୍ଥାନ ଅଦଳବଦଳ (Cross over) କରି ସଙ୍କେତ ଲେଖାଯାଏ ।
ଉଦାହରଣ :
କେତୋଟି ଆୟନର ନାମ ଓ ପ୍ରତୀକ/ସଙ୍କେତ
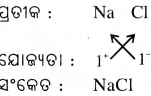
ମିଥେନ୍ ର ସଂକେତ :

![]()
(iii) ,କ୍ୟାନ୍ସିୟମ୍ କ୍ଲୋରାର ସଂକେତ :

(vi) ମ୍ୟାଟେ ସିୟମ୍ ଅକ୍ସାଇଡ଼୍ର ସଂକତ
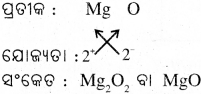
(v) କ୍ୟାଲ୍ ସିୟମ୍ ହାଇଟ୍ରକ୍କର ସଂକେତ :
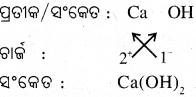
(vi) ସୋନିୟମ୍ ସଲ୍ଫେଟ୍ର ସଂକେଟ :
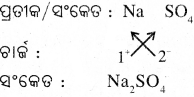
(vii) ଏମୋନିୟମ୍ କାବେର୍ବ ନେଟ୍ ର ସଂକେତ