Odisha State Board BSE Odisha 10th Class Physical Science Solutions Chapter 1 ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଓ ରାସାୟନିକ ସମୀକରଣ Textbook Exercise Questions and Answers.
BSE Odisha Class 10 Physical Science Solutions Chapter 1 ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଓ ରାସାୟନିକ ସମୀକରଣ
Question 1.
ନିମ୍ନରେ ଦର୍ଶାଯାଇଥିବା ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମ୍ବନ୍ଧରେ କେଉଁ ଉକ୍ତିଗୁଡ଼ିକ ଠିକ୍ ନୁହେଁ ?
2PbO (s) + C(s) → 2Pb(s) + CO2 (g)
(a) ଲେଡ୍ (Pb) ବିଜାରିତ ହେଉଛି ।
(b) କାର୍ବନ୍ ଡାଇଅକ୍ସାଇଡ୍ (CO2) ଜାରିତ ହେଉଛି
(c) କାର୍ବନ୍ (C) ଜାରିତ ହେଉଛି
(d) ଲେଡ୍ ଅକ୍ସାଇଡ୍ (PbO) ବିଚ୍ଚାରିତ ହେଉଛି
(i) (a) ଓ (b)
(ii) (a) ଓ (c)
(iii) (a), (b) ଓ (c)
(iv) ସମସ୍ତ ରକ୍ତ୍ରି
Answer:
(i) (a) ଓ (b)
Question 2.
Fe2O3 + 2Al → Al2O3 + 2Fe
ଉପରେ ଦିଆଯାଇଥିବା ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଟି ଏକ
(a) ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟା
(b) ଦ୍ଵୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା
(c) ବିଘଟନ ପ୍ରତିକ୍ରିୟ
(d) ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା
Answer:
(d) ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା
Question 3.
ଲଘୁ ହାଇଡ୍ରୋକ୍ଲୋରିକ୍ ଏସିଡ୍କୁ ଲୁହାଗୁଣ୍ଡରେ ମିଶାଇଲେ କ’ଣ ଘଟେ ? ଠିକ୍ ଉତ୍ତରରେ ଟିକ୍ (✓ ) ଚିହ୍ନ ଦିଅ
(a) ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ଓ ଆଇରନ୍ କ୍ଲୋରାଇଡ୍ ଉତ୍ପନ୍ନ ହୁଏ ।
(b) ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ଓ ଆଇରନ୍ କ୍ଲୋରାଇଡ୍ ଉତ୍ପନ୍ନ ହୁଏ ।
(c) କ୍ଲୋରିନ୍ ଗ୍ୟାସ୍ ଓ ଆଇରନ୍ ହାଇଡ୍ରିକସାଇଡ୍ ଉତ୍ପନ୍ନ ହୁଏ ।
(d) ଲୌହ ଲବଣ ଓ ଜଳ ଉତ୍ପନ୍ନ ହୁଏ ।
Answer:
(a) ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ଓ ଆଇରନ୍ କ୍ଲୋରାଇଡ୍ ଉତ୍ପନ୍ନ ହୁଏ ।
![]()
Question 4.
ଏକ ସମତୁଲ ରାସାୟନିକ ସମୀକରଣ କ’ଣ ? ରାସାୟନିକ ସମୀକରଣଗୁଡ଼ିକ କାହିଁକି ସମତୁଲ ହେବା ଉଚିତ ?
Answer:
ସମତୁଲ ରାସାୟନିକ ସମୀକରଣ
(i) ଯେଉଁ ରାସାୟନିକ ସମୀକରଣରେ ବାମପାର୍ଶ୍ଵରେ ଥିବା ପ୍ରତ୍ୟେକ ମୌଳିକର ପରମାଣୁ ସଂଖ୍ୟା, ଦକ୍ଷିଣ ପାର୍ଶ୍ଵରେ ଥିବା ପ୍ରତ୍ୟେକ ମୌଳିକର ପରମାଣୁ ସଂଖ୍ୟା ସହ ସମାନ ହୋଇଥାଏ, ତାହାକୁ ସମତୁଲ ରାସାୟନିକ
(ii)ଡାଲଟନ୍ଙ୍କ ପରମାଣୁ ତତ୍ତ୍ବ ଅନୁସାରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମୟରେ ପରମାଣୁଗୁଡ଼ିକର ସୃଷ୍ଟି ହୁଏ ନାହିଁ କିମ୍ବା ବିନାଶ ଘଟେ ନାହିଁ । ଏକ ଅସମତୁଲ ସମୀକରଣରେ ଉଭୟ ପାର୍ଶ୍ଵର ପରମାଣୁଗୁଡ଼ିକର ମୋଟ ବସ୍ତୁତ୍ଵ
(iii) ବସ୍ତୁତ୍ୱ ସଂରକ୍ଷଣ ନିୟମ ଅନୁସାରେ କୌଣସି ଏକ ରାସାୟନିକ ସମୀକରଣ ଉତ୍ପାଦରେ ଥିବା ମୌଳିକଗୁଡ଼ିକର ମୋଟ ବସ୍ତୁତ୍ଵ ପ୍ରତିକାରକରେ ଥିବା ମୌଳିକଗୁଡ଼ିକର ମୋଟ ବସ୍ତୁତ୍ବ ସହିତ ନିଶ୍ଚୟ ସମାନ ରହିବ । ମୌଳିକର ମୋଟ ବସ୍ତୁତ୍ଵ ଏହାର ପରମାଣୁ ସଂଖ୍ୟା ଉପରେ ନିର୍ଭର କରୁଥିବାରୁ ରାସାୟନିକ ସମୀକରଣକୁ ସମତୁଲ କରିବାକୁ ପଡ଼ିଥାଏ ।
Question 5.
ନିମ୍ନଲିଖ ଉକ୍ତିଗୁଡ଼ିକୁ ରାସାୟନିକ ସମୀକରଣରେ ଲେଖୁ ସେଗୁଡ଼ିକ ସମତୁଲ କର ।
(a) ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ନାଇଟ୍ରୋଜେନ୍ ସହିତ ମିଳିତ ହେଲେ ଏମୋନିଆ ହୁଏ ।
ଉ : H2 + N2 – NH2 : ସୂଚକ ସମୀକରଣ
3H2(g) + N2(g) → 2NH3 (g) : ସମତୁଲ ସମୀକରଣ
(b) ହାଇଡ୍ରୋଜେନ୍ ସଲ୍ଫାଇଡ୍ ଗ୍ୟାସ୍ ବାୟୁରେ ଜଳିଲେ ଜଳ ଓ ସଲ୍ଫର୍ ଡାଇଅକ୍ସାଇଡ୍ ହୁଏ ।
ଉ : H2S + O2 → SO2 + H2O : ଅସମତୁଲ ସମୀକରଣ
2H2S (g) + 3O2(g) ) → 2SO2 (g) + 2H2O : ସମତୁଲ ସମୀକରଣ
(C) ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ ଓ ଏଲୁମିନିୟମ୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣର ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ହେଲେ ବେରିୟମ୍ ସଲ୍ଫେଟ୍ର ଅବକ୍ଷେପ ଏବଂ ଏଲୁମିନିୟମ୍ କ୍ଲୋରାଇଡ୍ ଦ୍ରବଣ ମିଳେ ।
ଉ : BaCl2 + Al2 (SO4)3 → BaSO4 + AICI3 : ଅସମତୁଲ ସମୀକରଣ
3BaCl2 (aq) + Al2 (SO4)3 → 3BaSO4 (s) + 2AICI3 (aq) : ସମତୁଲ ସମୀକରଣ
(d) ପୋଟାସିୟମ୍ ଜଳ ସହିତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରି ପୋଟାସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ ଓ ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ କରେ ।
ଉ : K + H2O → KOH + H2 : ଅସମତୁଲ ସମୀକରଣ
2K(s) + 2H2O (l) → 2KOH (l) + H2 (g) : ସମତୁଲ ସମୀକରଣ
Question 6.
ନିମ୍ନଲିଖ ରାସାୟନିକ ସମୀକରଣଗୁଡ଼ିକୁ ସମତୁଲ କର ।
(a) HNO3 + Ca(OH)2 → Ca(NO3)2 + H2O
ଉ : 2HNO3 + Ca(OH)2 → Ca (NO3)2 + H2O
(b) NaOH + H2SO4 → Na2SO4 + H2O
ଉ : 2NaOH + H2SO4 → Na2SO4 + 2H2O
(c) NaCl + AgNO2 → AgCl + NaNO3
ଉ : NaCl + AgNO2 → AgCl + NaNO3
(d) BaCl2 + H2SO4 → BaSO4 + HCI
ଉ : BaCl2 + H2SO4 → BaSO4 + 2HCI
Question 7.
ନିମ୍ନଲିଖ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଗୁଡ଼ିକ ପାଇଁ ସମତୁଲ ରାସାୟନିକ ସମୀକରଣ ଲେଖ ।
(a) କ୍ୟାଲସିୟମ୍ ହାଇଟ୍ରକ୍ସାଇଡ୍ + କାର୍ବନ୍ ଡାଇଅକ୍ସାଇଡ୍ → କ୍ୟାଲ୍ସିୟମ୍ କାର୍ବୋନେଟ୍ + ଜଳ
ଊ : Ca (OH)2 + CO2 → CaCO3 + H2O
(b) ଜିଙ୍କ୍ + ସିଲଭର୍ ନାଇଟ୍ରେଟ୍ – → ଜିଙ୍କ୍ ନାଇଟ୍ରେଟ୍ + ସିଲ୍ଭର୍
ଊ : Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
(C) ଏଲୁମିନିୟମ୍ + କପର୍ କ୍ଲୋରାଇଡ୍ → ଏଲୁମିନିୟମ୍ କ୍ଲୋରାଇଡ୍ + କପର
ଊ : 2Al + 3CuCl2 → 2AlCl3 + 3Cu
(d) ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ + ପୋଟାସିୟମ୍ ସଲଫେଟ୍ → ବେରିୟମ ସଲ୍ଫେଟ୍ + ପୋଟାସିୟମ୍ କ୍ଲୋରାଇଡ୍
ଉ : BaCl2 + K2SO4 → BaSO4 + 2KCI
Question 8.
![]()
କେଉଁ ପ୍ରକାରର ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସୂଚାଅ ।
(a) ଆଇରନ୍ ସଲ୍ଫାଇଡ୍ (କଠିନ) + ସଲ୍ଫ୍ୟୁରିକ୍ ଏସିଡ୍ (ଜଳୀୟ) → ଆଇରନ୍ ସଲ୍ଫେଟ୍ (ଜଳୀୟ) + ହାଇଡ୍ରୋଜେନ୍ ସଲ୍ଫାଇଡ୍ (ଗ୍ୟାସ୍)
ଉ : FeS (s) + H2SO4 (ag) → FeSO4 (aq) + H2S (g) (ଦ୍ୱୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା)
(b) ଜିଙ୍କ୍ କାର୍ବୋନେଟ୍ (କଠିନ) → ଜିଙ୍କ୍ ଅକସାଇଡ୍ (କଠିନ) + କାର୍ବନ୍ ଡାଇଅକ୍ସାଇଡ୍ (ଗ୍ୟାସ୍)
ଉ : ZnCO3 (s) → ZnO(s) + CO2 (g) (ଦ୍ୱୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା)
(c) ହାଇଡ୍ରୋଜେନ୍ (ଗ୍ୟାସ୍) + କ୍ଲୋରିନ୍ (ଗ୍ୟାସ୍) → ହାଇଡ୍ରୋଜେନ କ୍ଲୋରାଇଡ୍ (ଗ୍ୟାସ୍)
ଉ : H2(g) + Cl2 (g) → 2HCl (g) (ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟା)
(d) ମ୍ୟାଗ୍ନେସିୟମ (କଠିନ) + ହାଇଡ୍ରୋକ୍ଲୋରିକ୍ ଏସିଡ୍ (ଜଳୀୟ) → ମ୍ୟାଗ୍ନେସିୟମ୍ କ୍ଲୋରାଇଡ୍ (ଜଳୀୟ) + ହାଇଡ୍ରୋଜେନ୍ (ଗ୍ୟାସ୍)
ଉ : Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2(g) (ବିଘଟନ ପ୍ରତିକ୍ରିୟା)
![]()
Question 9.
ତାପଉତ୍ପାଦୀ ଓ ତାପଶୋଷୀ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କହିଲେ କ’ଣ ବୁଝ ? ଉଦାହରଣ ଦିଅ ।
Answer:
ତାପଉତ୍ପାଦୀ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା : ଯେଉଁ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଉତ୍ପାଦ ଉତ୍ପନ୍ନ ହେବା ସଙ୍ଗେ
ସଙ୍ଗେ ତାପ ନିର୍ଗତ ହୋଇଥାଏ, ତାହାକୁ ତାପ ଉତ୍ପାଦୀ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ ।
ଉଦାହରଣ:
(i) କ୍ୟାଲସିୟମ୍ ଅକ୍ସାଇଡ୍ର ଜଳ ସହିତ ତୀବ୍ର ପ୍ରତିକ୍ରିୟା ଘଟି ପ୍ରଚୁର ପରିମାଣର ତାପ ନିର୍ଗତ ହେବା ସଙ୍ଗେ
CaO(s) + H2O(l) → Ca(OH)2 (aq)
(କଲିଚୂନ) (ଶମିତ ଚୂନ)
(ii) ପ୍ରାକୃତିକ ଗ୍ୟାସ୍ର ଦହନ ଫଳରେ ଅଙ୍ଗାରକାମ୍ଳ ଓ ଜଳୀୟବାଷ୍ପ ସୃଷ୍ଟି ହେବା ସହିତ ପ୍ରଚୁର ତାପଶକ୍ତି ନିର୍ଗତ ହୋଇଥାଏ ।
CH4(g) + 2O2(g) → CO2(g) + 2H2O (g)
(iii) ଶ୍ଵାସକ୍ରିୟା ବା ଶ୍ୱସନ ପ୍ରକ୍ରିୟା ମଧ୍ୟ ଏକ ତାପ ଉତ୍ପାଦୀ ପ୍ରତିକ୍ରିୟା ଅଟେ । ପରିପାକ ପ୍ରକ୍ରିୟାରେ ଖାଦ୍ୟ ସରଳତର ପଦାର୍ଥରେ ପରିଣତ ହୁଏ । ଭାତ, ରୁଟି, ଆଳୁ ଇତ୍ୟାଦି ଶ୍ଵେତସାର ଜାତୀୟ ଖାଦ୍ୟରୁ ରୁ କୋଜ୍ (C6H12O6) ସୃଷ୍ଟି ହୁଏ । ଗ୍ଲ କୋଜ୍ ଆମ ଶରୀରର ଜୀବକୋଷ ମଧ୍ୟରେ ଥିବା ଅକ୍ସିଜେନ ସହିତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରେ ଏବଂ ଶରୀରକୁ ଶକ୍ତି ଯୋଗାଇଥାଏ ।
C6H12O6 (aq) + 6O2(aq) → 6CO2(aq) + 6H2O(l) + energy
ତାପଶୋଷୀ ପ୍ରତିକ୍ରିୟା: ଯେଉଁ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ତାପଶକ୍ତି ଶୋଷିତ ହୋଇଥାଏ, ତାହାକୁ ତାପଶୋଷୀ ବା ତାପଗ୍ରାହୀ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ ।
ଉଦାହରଣ:
ବେରିୟମ୍ ହାଇଡ୍ରୋକ୍ସାଇଡ୍ ସହିତ ଏମୋନିୟମ୍ କ୍ଲୋରାଇଡ୍ ମିଶିଲେ, ତାପଶକ୍ତି ଶୋଷିତ ହୋଇଥାଏ ଏବଂ ଅନ୍ୟାନ୍ୟ ଯୌଗିକମାନ ସୃଷ୍ଟି ହୁଏ ।
Ba (OH)2 + 2 NH4Cl → 2NH4OH + BaCl2
Question 10.
ଶ୍ଵାସକ୍ରିୟାକୁ କାହିଁକି ଏକ ତାପଉତ୍ପାଦୀ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଭାବରେ ଧରାଯାଇଥାଏ ? ବୁଝାଅ ।
Answer:
(i) ଶ୍ଵାସକ୍ରିୟା ମାଧ୍ୟମରେ ଆମ ଶରୀରର ଜୀବକୋଷଗୁଡ଼ିକ ମଧ୍ୟରେ ସଞ୍ଚିତ ଥିବା ଅକ୍ସିଜେନ୍ (02) ସହିତ ରକ୍ତରେ ଥିବା ଗ୍ଲୁକୋଜର ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ଅଙ୍ଗାରକାମ୍ଳ ଓ ତାପଶକ୍ତି ଉତ୍ପନ୍ନ ହୋଇଥାଏ ।
(ii) ଏହା ଆମ ଶରୀରକୁ କାର୍ଯ୍ୟକାରୀ ଶକ୍ତି ଯୋଗାଇଥାଏ । ତେଣୁ ଶ୍ଵାସକ୍ରିୟାକୁ ଏକ ତାପ ଉତ୍ପାଦୀ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଭାବରେ ଧରାଯାଇଥାଏ ।
C6H12O6(aq) + 6O2 (aq) → 6CO2(aq) + 6H2O (l) + energy
Question 11.
ବିଘଟନ ପ୍ରତିକ୍ରିୟାକୁ କାହିଁକି ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାର ବିପରୀତ ବୋଲି କୁହାଯାଏ ? ଏହି ଦୁଇଟି ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ପାଇଁ ରାସାୟନିକ ସମୀକରଣ ଲେଖ ।
Answer:
(i) ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାରେ ଦୁଇ ବା ଅଧ୍ଵ ମୌଳିକ କିମ୍ବା ଯୌଗିକ ସଂଯୁକ୍ତ ହୋଇ ଏକ ନୂତନ ଯୌଗିକ ଉତ୍ପନ୍ନ ହୁଏ ।
(ii) କିନ୍ତୁ ବିଘଟନ ପ୍ରତିକ୍ରିୟାରେ ଗୋଟିଏ ଯୌଗିକ ବିଘଟିତ ହୋଇ ଏକାଧ୍ଵ ସରଳତର ମୌଳିକ କିମ୍ବା ଯୌଗିକ ସୃଷ୍ଟି କରନ୍ତି । ତେଣୁ ବିଘଟନ ପ୍ରତିକ୍ରିୟାକୁ ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାର ବିପରୀତ ବୋଲି କୁହାଯାଇଥାଏ । ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟା: ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟା : 2H2(g) + O2(g) → 2H2O (l)
ବିଘଟନ ପ୍ରତିକ୍ରିୟା : CaCO3 (s) → CaO(s) + CO2(g)
Question 12.
ତାପ, ଆଲୋକ କିମ୍ବା ବିଦ୍ୟୁତ୍ ଶକ୍ତି ପ୍ରୟୋଗ ଦ୍ବାରା ସମ୍ପାଦିତ ହେଉଥିବା ପ୍ରତ୍ୟେକ ବିଘଟନ ପ୍ରତିକ୍ରିୟା ପାଇଁ ରାସାୟନିକ ସମୀକରଣ ଲେଖ ।
Answer:
(i) ତାପ ପ୍ରୟୋଗ ଦ୍ଵାରା ଘଟୁଥିବା ବିଘଟନ ପ୍ରତିକ୍ରିୟା:
କ୍ୟାଲସିୟମ୍ କାର୍ବୋନେଟ୍କୁ ଉତ୍ତପ୍ତ କଲେ ଏହା ବିଘଟିତ ହୋଇ କ୍ୟାଲ୍ସିୟମ୍ ଅକ୍ସାଇଡ଼ ଓ କାର୍ବନ
ଡାଇଅକ୍ସାଇଡ଼ର ଉତ୍ପନ୍ନ କରେ ।
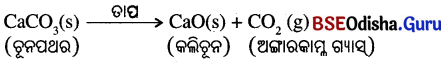
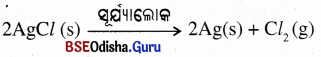
(ii) ସିଲଭର୍ କ୍ଲୋରାଇଡ଼ ସୂର୍ଯ୍ୟାଲୋକ ଉପସ୍ଥିତିରେ ବିଘଟିତ ହୋଇ ସିଲଭର୍ ଓ କ୍ଲୋରିନ୍ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ କରେ ।
![]()
(iii) ବିଦ୍ୟୁତ୍ ଶକ୍ତି ପ୍ରୟୋଗଦ୍ଵାରା ଘଟୁଥିବା ବିଘଟନ ପ୍ରତିକ୍ରିୟା:
ବିଦ୍ୟୁତ୍ ଶକ୍ତି ପ୍ରୟୋଗଦ୍ଵାରା ଜଳ ବିଘଟିତ ହୋଇ ଉଦ୍ଜାନ ଗ୍ୟାସ୍ ଓ ଅମ୍ଳଜାନ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ କରେ ।
![]()
Question 13.
ବିସ୍ଥାପନ ଓ ଦ୍ଵୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା ମଧ୍ୟରେ ପାର୍ଥକ୍ୟ କ’ଣ ? ଏହି ଦୁଇ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ପାଇଁ
Answer:
ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାରେ ଗୋଟିଏ ମୌଳିକ କୌଣସି ଏକ ଯୌଗିକର ମୌଳିକକୁ ଅପସାରଣ କରେ ।
Zn(s) + CuSO4 (aq) → ZnSO4 (aq) + Cu(s)
Fe(s) + Cu SO4 (aq) → FeSO4(aq) + Fe (s)
ଦ୍ୱୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାରେ ପ୍ରତିକାରକ ଦୁଇଟି ମଧ୍ଯରେ ଆୟନ ବିନିମୟ ଘଟିଥାଏ ।
AgNO3(aq) + NaCl (aq) → AgCl (s)↓ + NaNO3(aq)
BaCl2(aq) + Na2SO4(aq) → BaSO4(s) ↓ + 2NaCl (aq)
Question 14.
ସିଲ୍ଭର୍ ଶୋଧନରେ, କପର୍ ଧାତୁ ଦ୍ବାରା ସିଲ୍ଭର୍ ନାଇଟ୍ରେଟ୍ ଦ୍ରବଣରୁ ସିଲ୍କଭରକୁ ଅପସାରଣ କରି ସିଲ୍ଭର୍ ନିଷ୍କାସନ କରାଯାଏ । ଏହା ସହିତ ସମ୍ପୃକ୍ତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଟିକୁ ଲେଖ ।
Answer:
କପର ଓ ସିଲ୍ଭର୍ ନାଇଟ୍ରେଟ୍ ଦ୍ରବଣ ମଧ୍ୟରେ ପ୍ରତିକ୍ରିୟା ଘଟିଲେ କପର ନାଇଟ୍ରେଟ୍ ଓ ଧାତବ ସିଲ୍ଭର୍ ସୃଷ୍ଟିହୁଏ ।
Cu(s) + 2AgNO3(aq) → Cu(NO3)2(aq) + 2Ag (s) ↓
କପର + ସିଲଭର ନାଇଟ୍ରେଟ୍ → କପର ନାଇଟ୍ରେଟ୍ + ସିଲଭର
![]()
Question 15.
ଅବକ୍ଷେପଣ ପ୍ରତିକ୍ରିୟା କହିଲେ କଣ ବୁଝ ? ଉଦାହରଣ ଦେଇ ବୁଝାଅ ।
Answer:
ଅବକ୍ଷେପଣ ପ୍ରତିକ୍ରିୟା :
ଅଧିକାଂଶ ଦ୍ଵୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାରେ ଜଳୀୟ ଦ୍ରବଣରେ ଦୁଇଟି ଆୟନିୟ ଯୌଗିକ ମଧ୍ୟରେ ପ୍ରତିକ୍ରିୟା ଘଟି ଏକ ଅଦ୍ରବଣୀୟ ଉତ୍ପାଦନ ସୃଷ୍ଟି କରିଥାଏ । ଏହାକୁ ଅବକ୍ଷେପ କୁହାଯାଏ ।
ଯେଉଁ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଏକ ଅଦ୍ରବଣୀୟ ଉତ୍ପାଦ ବା ଅବକ୍ଷେପ ସୃଷ୍ଟି ହୁଏ, ତାହାକୁ ଅବକ୍ଷେପଣ ପ୍ରତିକ୍ରିୟା (Precipitation reaction) କୁହାଯାଏ ।
ଉଦାହରଣ:
ସୋଡ଼ିୟମ୍ ସଲଫେଟ୍ ସହିତ ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ ଦ୍ରବଣ ମିଶିଲେ ଏକ ଧଳା ଅଦ୍ରବଣୀୟ ପଦାର୍ଥ ସୃଷ୍ଟି ହୋଇଥାଏ । ଏହି ପଦାର୍ଥଟି ହେଉଛି ବେରିୟମ ସଲ୍ଫେଟ୍ । ଉତ୍ପନ୍ନ ହୋଇଥିବା ଏହି ଅଦ୍ରବଣୀୟ ପଦାର୍ଥକୁ ଅବକ୍ଷେପ କହନ୍ତି ।
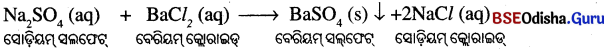
Question 16.
ଅକ୍ସିଜେନ୍ ଗ୍ରହଣ ଓ ଅକ୍ସିଜେନ୍ ପରିହାର ଦୃଷ୍ଟିରୁ ନିମ୍ନଲିଖତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଦୁଇଟିକୁ ବୁଝାଅ । ପ୍ରତ୍ୟେକ ପାଇଁ ଦୁଇଟି ଲେଖାଏଁ ଉଦାହରଣ ଦିଅ । (a) ଜାରଣ, (b) ବିଜାରଣ
Answer:
ଜାରଣ (Oxidation) : ଯେଉଁ ପ୍ରତିକ୍ରିୟାରେ ପ୍ରତିକାରକ ଅକ୍ସିଜେନ୍ ଗ୍ରହଣ କରେ କିମ୍ବା ହାଇଡ୍ରୋଜେନ୍ ହରାଏ ତାହାକୁ ଜାରଣ କୁହାଯାଏ ।
କପର ସହିତ ଅକ୍ସିଜେନର ରାସାୟନିକ ସଂଯୋଗ ଘଟି କପର ଅକ୍ସାଇଡ୍ ଉତ୍ପନ୍ନ ହୋଇଥାଏ ।
ଉଦାହରଣ:
(i) କପର ସହିତ ଅକ୍ସିଜେନର ରାସାୟନିକ ସଂଯୋଗ ଘଟି କପର ଅକ୍ସାଇଡ୍ ଉତ୍ପନ୍ନ ହୋଇଥାଏ ।
![]()
ଏଠାରେ କପର ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଅକ୍ସିଜେନ୍ ଗ୍ରହଣ କରିଥାଏ ।
(ii) ମ୍ୟାଗ୍ନେସିୟମ୍ ପାତ ବାୟୁରେ ଉଜ୍ଜ୍ଵଳ ଭାବରେ ଜଳି ଏକ ଧଳା ପଦାର୍ଥ, ମ୍ୟାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ୍ ସୃଷ୍ଟି କରେ ।
![]()
(b) ବିଜାରଣ (Reduction): ଯେଉଁ ପ୍ରତିକ୍ରିୟାରେ ପ୍ରତିକାରକ ଅକ୍ସିଜେନ୍ ହରାଏ କିମ୍ବା ହାଇଡ୍ରୋଜେନ୍ ଗ୍ରହଣ କରେ ତାହାକୁ ବିଜାରଣ କୁହାଯାଏ ।
ଉଦାହରଣ:
(i) ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍କୁ ଉତ୍ତପ୍ତ କପର ଅକ୍ସାଇଡ୍ ଉପରେ ପ୍ରବାହିତ କଲେ, କପର ଅକସାଇଡ୍ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମୟରେ ବିଜାରିତ ହୋଇ ଅକ୍ସିଜେନ ହରାଇଥାଏ ।
![]()
(ii) ଜିଙ୍କ୍ ଅକ୍ସାଇଡ୍ର କାର୍ବନ ସହିତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ବେଳେ ଜିଙ୍ଗ୍ ଅକ୍ସାଇଡ୍ , ଅକ୍ସିଜେନ୍ ହରାଇଥାଏ ।
ZnO + C → Zn + CO
Question 17.
ଏକ ଉଜ୍ଜଳ ବାଦାମୀ ବର୍ଷର ମୌଳିକ ‘X’କୁ ଗରମ କଲେ କଳା ହୋଇଯାଏ । ମୌଳିକ ‘X’ ଏବଂ ସୃଷ୍ଟି ହୋଇଥିବା କଳା ଯୌଗିକର ନାମ ଲେଖ ।
Answer:
ଏକ ଉଜ୍ଜ୍ବଳ ବାଦାମୀ ବର୍ଷର ମୌଳିକ ‘X’କୁ ଗରମ କଲେ କଳା ହୋଇଯାଏ । ମୌଳିକ ‘X’ ର ନାମ କପର ଏବଂ ସୃଷ୍ଟି ହୋଇଥିବା କଳା ଯୌଗିକର ନାମ କପର (II) ଅକ୍ସାଇଡ୍ ।
2Cu + O2 → 2CuO
Question 18.
ଲୌହ ନିର୍ମିତ ପଦାର୍ଥଗୁଡ଼ିକ ଉପରେ ଆମେ କାହିଁକି ରଙ୍ଗ ଲଗାଇଥାଉ ?
Answer:
(i) ଲୌହ ନିର୍ମିତ ପଦାର୍ଥ ଯଦି କିଛି ଦିନ ପାଇଁ ବାହାରେ ପଡ଼ିରହେ ତେବେ ତା’ଉପରେ ଏକ ଲୋହିତ-ବାଦାମୀ
ରଙ୍ଗର ପ୍ରଲେପ ମାଡ଼ିଯାଏ । ଏହି ପ୍ରାକୃତିକ ପ୍ରକ୍ରିୟାକୁ ‘ଲୁହାରେ କଳଙ୍କି ଲାଗିବା’’ କୁହାଯାଏ ।
(ii) ଲୁହା ବାୟୁମଣ୍ଡଳର ଜଳୀୟବାଷ୍ପ ସହ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରି ଲୌହ ଅକ୍ସାଇଡ୍ ସୃଷ୍ଟି କରେ । ଏହି ଧାତବ ଅକ୍ସାଇଡ୍ ଲୁହା ଉପରେ ଏକ ଲୋହିତ ବାଦାମୀ ରଙ୍ଗର ପ୍ରଲେପ ସୃଷ୍ଟି କରିଥାଏ । ଏହା ଫଳରେ ଲୌହ ନିର୍ମିତ ପଦାର୍ଥର ଧୀରେ ଧୀରେ କ୍ଷୟ ଘଟିଥାଏ ଏବଂ ଲୁହା ତା’ର ଦୀପ୍ତି ହରାଇଥାଏ ।
(iii) ତେଣୁ ଲୌହ ନିର୍ମିତ ପଦାର୍ଥଟି ବାୟୁମଣ୍ଡଳରେ ଜଳୀୟବାଷ୍ପ ସଂସ୍ପର୍ଶରେ ନ ଆସିବା ପାଇଁ ତା’ଉପରେ ରଙ୍ଗର ପ୍ରଲେପ ଦିଆଯାଇଥାଏ ।
ତୈଳ ଓ ଚର୍ବିଯୁକ୍ତ ଖାଦ୍ୟସାମଗ୍ରୀ ଥିବା ଡବା ମଧ୍ୟରେ ନାଇଟ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ କାହିଁକି ପ୍ରବେଶ କରାଯାଇଥାଏ ?
Question 19.
ତୈଳ ଓ ଚର୍ବିଯୁକ୍ତ ଖାଦ୍ୟ ସାମଗ୍ରୀ ଡବା ମଧ୍ୟରେ ଥିବା ବାୟୁ ସଂସ୍ପର୍ଶରେ ଆସି ଜାରିତ ହୋଇଥାଏ ଏବଂ ସେଥୁରୁ ରହଣିଆ ଗନ୍ଧ ବାହାରିଥାଏ ।
Answer:
(i) ତୈଳ ଓ ଚର୍ବିଯୁକ୍ତ ଖାଦ୍ୟ ସାମଗ୍ରୀ ଡବା ମଧ୍ୟରେ ଥିବା ବାୟୁ ସଂସ୍ପର୍ଶରେ ଆସି ଜାରିତ ହୋଇଥାଏ ଏବ ସେଥୁରୁ ରହଣିଆ ଗନ୍ଧ ବାହାରିଥାଏ । ତେଣୁ ଜାରଣକୁ ପ୍ରତିହତ କରିବା ପାଇଁ ଖାଦ୍ୟ ସାମଗ୍ରୀ ଥିବା ଡବ ମଧ୍ୟରେ ବାୟୁ ବଦଳରେ ନାଇଟ୍ରୋଜେନ ଗ୍ୟାସ୍ ବ୍ୟବହାର କରାଯାଇଥାଏ । ଏହାଫଳରେ ଖାଦ୍ୟ ସାମଗ୍ରୀ ବହୁତ ଦିନ ପର୍ଯ୍ୟନ୍ତ ସଂରକ୍ଷିତ ହୋଇ ରହିଥାଏ ।
(ii) ଏହାଫଳରେ ଖାଦ୍ୟ ସାମଗ୍ରୀ ବହୁତ ଦିନ ପର୍ଯ୍ୟନ୍ତ ସଂରକ୍ଷିତ ହୋଇ ରହିଥାଏ ।
![]()
Question 20.
ପ୍ରତ୍ୟେକ ପାଇଁ ଉଦାହରଣ ଦେଇ ନିମ୍ନଲିଖତ ପ୍ରତିକ୍ରିୟାକୁ ବୁଝାଅ ।
ସଂକ୍ଷାରଣ (Corrosion):
(i) ଏକ ଲୌହ ନିର୍ମିତ ଦ୍ରବ୍ୟ ନୂତନ ଅବସ୍ଥାରେ ଉଜ୍ଜ୍ଵଳ ଓ ମସୃଣ ହୋଇଥାଏ । କିନ୍ତୁ ଏହା କିଛି ଦିନ ବାହାରେ ପଡ଼ିରହିଲେ, ଏହା ଉପରେ ଏକ ଲୋହିତ-ବାଦାମୀ ରଙ୍ଗର ପ୍ରଲେପ ମାଡ଼ିଯାଏ । ଏହି ପ୍ରାକୃତିକ ‘‘ ପ୍ରକ୍ରିୟାକୁ ‘‘ଲୁହାରେ କଳଙ୍କି ଲାଗିବା’’ କୁହାଯାଏ ।
(ii) ଯେତେବେଳେ ଏକ ଧାତୁ ତାକୁ ଘେରି ରହିଥିବା ଉପାଦାନ ଗୁଡ଼ିକ (ଯଥା – ଜଳୀୟବାଷ୍ପ, ଅମ୍ଳ ଇତ୍ୟାଦି) ସହିତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରେ, ସେତେବେଳେ ଧାତୁଟିର ଧୀରେ ଧୀରେ କ୍ଷୟ ଘଟିଥାଏ । ଧାତୁର ଏହି କ୍ଷୟ ହେବା ପ୍ରକ୍ରିୟାକୁ ସଂକ୍ଷାରଣ ବା କ୍ରମକ୍ଷୟ କୁହାଯାଏ ।
(iii) ସିଲ୍ ଭର ଉପରେ ପଡୁଥିବା କଳା ଆସ୍ତରଣ ଓ କପର ଉପରେ ପଡୁଥିବା ସବୁଜ ଆସ୍ତରଣ ହେଉଛି ସଂକ୍ଷାରଣର ଉଦାହରଣ ।
(iv) ସଂକ୍ଷାରଣ ହେତୁ ମଟରଗାଡ଼ି, ପୋଲ, ଲୁହାବାଡ଼, ଜାହାଜ ଏବଂ ଧାତୁ ନିର୍ମିତ ସମସ୍ତ ବସ୍ତୁ ବିଶେଷକରି ଲୌହ ନିର୍ମିତ ବସ୍ତୁଗୁଡ଼ିକର କ୍ଷୟ ଘଟିଥାଏ !
(b) ରହୁଣିଆ ଅବସ୍ଥା (Rancidity):
(i) ବହୁତ ଦିନ ଧରି ରହିଯାଇଥିବା ଚର୍ବି ଏବଂ ତେଲ ବାୟୁ ସଂସ୍ପର୍ଶରେ ଆସି ଜାରିତ ହୋଇଥାଏ । ଏହାଫଳରେ ତା’ର ଗନ୍ଧ ଓ ସ୍ବାଦ ବଦଳିଯାଇଥାଏ । ତହିଁରୁ ରହଣିଆ ଗନ୍ଧ ବାହାରୁଛି ବୋଲି କୁହାଯାଏ । ଏହାକୁ ପଦାର୍ଥର ସଢ଼ା ଅବସ୍ଥା କୁହାଯାଏ ।
(ii) ଯେଉଁ ପଦାର୍ଥ ଜାରଣକୁ ନିରୋଧ କରେ ତାକୁ ପ୍ରତିଜାରକ (Antioxidant) କହନ୍ତି । ଖାଦ୍ୟ ସାମଗ୍ରୀରେ ସାଧାରଣତଃ ପ୍ରତିଜାରକକୁ ମିଶାଇ ସେଗୁଡ଼ିକୁ ବହୁଦିନ ପର୍ଯ୍ୟନ୍ତ ସଂରକ୍ଷଣ କରାଯାଇଥାଏ ।
(iii) ବାୟୁରୋଧୀ ପାତ୍ରରେ ଖାଦ୍ୟପଦାର୍ଥ ରଖେଲେ ଜାରଣ ପ୍ରକ୍ରିୟା ମନ୍ଥର ହୁଏ । ଏହାଫଳରେ ସେଗୁଡ଼ିକର ସଂରକ୍ଷଣ ସହଜ ହୋଇଥାଏ । ଜାରଣକୁ ପ୍ରତିହତ କରିବାପାଇଁ ନାଇଟ୍ରୋଜେନ୍ ଗ୍ୟାସ୍କୁ ମଧ୍ୟ ଖାଦ୍ୟ ମଧ୍ୟରେ ପୁରାଯାଇଥାଏ ।
ପ୍ରଣ୍ଠ| ଚ୍ ଳ 1 ଓଙତ୍ତର:
Question 1.
ମ୍ୟାଗ୍ନେସିୟମ୍ ପାତକୁ ବାୟୁରେ ଜଳାଇବା ପୂର୍ବରୁ କାହିଁକି ସଫାକରିବା ଉଚିତ ?
Answer:
ମ୍ୟାଗ୍ନେସିୟମ୍ ଏକ କ୍ରିୟାଶୀଳ ଧାତୁ ହୋଇଥିବାରୁ ଏହା ଅମ୍ଳଜାନ ସହ ପ୍ରତିକ୍ରିୟା କରି ମ୍ୟାଗ୍ନେସିୟମ୍ ପାତ ବାୟୁରେ ଜଳିନଥାଏ । ତେଣୁ ମ୍ୟାଗ୍ନେସିୟମ ପାତକୁ ବାୟୁରେ ଜଳାଇବା ପୂର୍ବରୁ ସଫା କରାଯାଇଥାଏ ।
Question 2.
ନିମ୍ନଲିଖତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଗୁଡ଼ିକ ପାଇଁ ସମତୁଲ ସମୀକରଣ ଲେଖ ।
(i) ହାଇଡ୍ରୋଜେନ୍ + କ୍ଲୋରିନ୍ → ହାଇଡ୍ରୋକର୍ କ୍ଲୋରାଇଡ୍
ଉ : H2 + Cl2 → 2HCI
(ii) ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ + ଏଲୁମିନିୟମ୍ ସଲ୍ଫେଟ୍ → ବେରିୟମ୍ ସଲ୍ଫେଟ୍ + ଏଲୁମିନିୟମ୍ କ୍ଲୋରାଇଡ
ଉ : 3BaCl2 + Al2 (SO4)3 → 3 BaSO4 + 2AlCl3
(iii) ସୋଡ଼ିୟମ୍ + ଜଳ → ସୋଡ଼ିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ + ହାଇଡ୍ରୋଜେନ୍
ଉ : 2Na + 2H2O → 2NaOH + H2
Question 3.
ନିମ୍ନଲିଖ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଗୁଡ଼ିକ ପାଇଁ ଅବସ୍ଥା ପ୍ରତୀକ ସହିତ ସମତୁଲ ରାସାୟନିକ ସମୀକରଣ ଲେଖ ।
(i) ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ ଓ ସୋଡ଼ିୟମ୍ ସଲ୍ଫେଟ୍ରର ଜଳୀୟ ଦ୍ରବଣ ଦୁଇଟି ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରି ଅଦ୍ରବଣୀୟ ବେରିୟମ୍ ସଲ୍ଫେଟ୍ ଓ ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ ଦ୍ରବଣ ପ୍ରଦାନ କରନ୍ତି ।
ଉ : BaCl2 (aq) + Na2SO4 (aq) → BaSO4(s) + 2NaCl (aq)
(ii) ସୋଡ଼ିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ଼ର ଜଳୀୟ ଦ୍ରବଣ ହାଇଡ୍ରୋକ୍ଲୋରିକ୍ ଏସିଡ୍ର ଜଳୀୟ ଦ୍ରବଣ ସହିତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରି ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ ଦ୍ରବଣ ଓ ଜଳ ଉତ୍ପନ୍ନ କରନ୍ତି ।
ଉ :
NaOH(aq) + HCl (aq) → NaCl (aq) + H2O (l)
Question 4.
ପଦାର୍ଥ ‘X’ ର ଏକ ଦ୍ରବଣ କାନ୍ଥକୁ ଧଉଳାଇବା ପାଇଁ ବ୍ୟବହାର କରାଯାଇଛି ।
(କ) ପଦାର୍ଥ ‘X’ ର ନାମ କ’ଣ ଏବଂ ତା’ର ସଂକେତ ଲେଖ ।
ଉ : ପଦାର୍ଥ ‘X’ ର ନାମ କ୍ୟାଲ୍ସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ ଏବଂ ଏହାର ସଂକେତ ହେଉଛି Ca(OH)2 ।
(ଖ) CO2, ସହିତ ପଦାର୍ଥ ‘X’ର ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଟି ଲେଖ ।
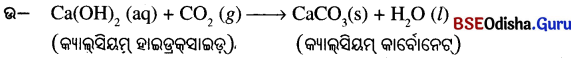
Question 5.
“ତୁମ ପାଇଁ କାମ 1.7 ରେ ଗୋଟିଏ ପରୀକ୍ଷାନଳୀରେ ସଂଗୃହୀତ ଗ୍ୟାସ୍ ପରିମାଣ ଅନ୍ୟ ପରୀକ୍ଷା ନଳୀରେ ସଂଗୃହୀତ ଗ୍ୟାସ୍ର ପରିମାଣର ଦୁଇଗୁଣ କାହିଁକି ? ଏହି ଦୁଇଟି ଗ୍ୟାସ୍ର ନାମ ଲେଖ ।
Answer:
ଅମ୍ଳୀକୃତ ଜଳରେ ବିଦ୍ୟୁତ୍ ଶକ୍ତି ପ୍ରବାହିତ ହେଲେ ଜଳ ଅଣୁ ବିଘଟିତ ହୋଇ H2, ଏବଂ O2, ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ କରେ । ଏହି ଦୁଇ ଗ୍ୟାସ୍ର ଅନୁପାତ ଯଥାକ୍ରମେ 2 : 1 । ତେଣୁ ଗୋଟିଏ ପରୀକ୍ଷାନଳୀରେ ସଂଗୃହୀତ ଗ୍ୟାସ୍ ପରିମାଣ ଅନ୍ୟ ପରୀକ୍ଷାନଳୀରେ ସଂଗୃହୀତ ଗ୍ୟାସ୍ ପରିମାଣର 2 ଗୁଣ ।
![]()
![]()
Question 6.
ଗୋଟିଏ ଲୁହାକଣ୍ଟାକୁ କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣରେ ବୁଡ଼ାଇଲେ, ଦ୍ରବଣର ରଙ୍ଗରେ ପରିବର୍ତ୍ତନ ଘଟେ କାହିଁକି ?
Answer:
ଲୁହାକଣ୍ଟାର କପର ସଲ୍ଫେଟ୍ ଦ୍ରବଣ ସହିତ ବିସ୍ଥାପନ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ଆଇରନ ସଲଫେଟ୍ ଦ୍ରବଣ ଓ କପର ସୃଷ୍ଟି ହୁଏ । ଏହି ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାରେ ଅଧିକ କ୍ରିୟାଶୀଳ ମୌଳିକ ଲୁହା କମ୍ କ୍ରିୟାଶୀଳ ମୌଳିକ କପରକୁ ନୀଳରଙ୍ଗର ତୀବ୍ରତାରେ ହ୍ରାସ ଘଟେ । ଲାଲ୍ କପର ଧାତୁ ଲୁହାକଣ୍ଟା ଉପରେ ଜମାହୁଏ । ଫେରସ୍ ଆୟନ (Fe2+) ସୃଷ୍ଟି ହେବା ଯୋଗୁଁ ନୀଳରୁ ଇଷତ୍ ସବୁଜ ରଙ୍ଗକୁ ପରିବର୍ତ୍ତିତ ହୁଏ ।
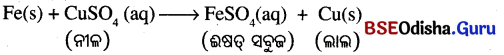
Question 7.
ତୁମପାଇଁ କାମ: 1.10 ର ଉଦାହରଣ ଭିନ୍ନ ଅନ୍ୟ ଏକ ଦ୍ୱୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା ପାଇଁ ଉଦାହରଣ ଦିଅ ।
Answer:
ଦ୍ୱୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାର ଅନ୍ୟ ଏକ ଉଦାହରଣ ହେଲା
NaCl (aq) + AgNO3 (aq) → NaNO3(aq) + AgCl (s) ↓
Question 8.
ନିମ୍ନଲିଖ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଗୁଡ଼ିକରେ କେଉଁଗୁଡ଼ିକ ଜାରିତ ହୋଇଛି ଏବଂ ହୋଇଛି ତାହା ସୂଚାଅ ।
Answer:
(i) 4Na(s) + O2(g) → 2Na2O(s)
(ii) CuO(s) + H2(g) → Cu(s) + H2O (l)
ମିଳିମିଶି କରିତ୍।
ତୁମ ନିଜର ସୂଚକ ପ୍ରସ୍ତୁତ କର :
- ଚାରୋଟି ବିକର୍ ନିଅ ଏବଂ ସେଗୁଡ଼ିକୁ A, B, C ଓ D ଭାବରେ ନାମାଙ୍କିତ କର ।
- 25 ମିଲି ଲି. ଲେଖାଏଁ ଜଳ A, B ଓ C ବିକର୍ରେ ଏବଂ କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣ D ବିକର୍ରେ ରଖ ।
- ଦୁଇ ଚାମଚ ଲେଖାଏଁ ପୋଟାସିୟମ୍ ସଲ୍ଫେଟ୍, ଏମୋନିୟମ୍ ନାଇଟ୍ରେଟ୍, ନିର୍ଜଳ କପର୍ ସଲ୍ଫେଟ୍ ଏବଂ ସରୁ ଲୁହାଗୁଣ୍ଡ ଯଥାକ୍ରମେ A, B, C ଓ Ð
- ବିକର୍ରେ ମିଶାଅ ଏବଂ ପ୍ରତ୍ୟେକ ମିଶ୍ରଣକୁ ଘାଣ୍ଟି ଦିଅ । ସର୍ବଶେଷରେ ପ୍ରତ୍ୟେକ ମିଶ୍ରଣର ତାପମାତ୍ରା ମାପ ଏବଂ ଲେଖୁ ରଖ ।
- କେଉଁ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଗୁଡ଼ିକ ତାପଉତ୍ପାଦୀ ଏବଂ କେଉଁଗୁଡ଼ିକ ତାପଶୋଷୀ ନିର୍ଣ୍ଣୟ କର ।
- ଉ – ଛାତ୍ରଛାତ୍ରୀମାନେ ଶିକ୍ଷକଙ୍କ ସହାୟତାରେ ପ୍ରସ୍ତୁତ କରିବେ ।
କାର୍ଯ୍ୟାବଳୀ (ACTIVITY):
କର୍ଯ୍ୟାବଳୀ-1 (Activity-1)
2 ସେ.ମି. ଲମ୍ବ ଏକ ମ୍ୟାଗ୍ନେସିୟମ୍ର ପତଳା ପାତକୁ
ଏହାର ଏକ ପାର୍ଶ୍ଵକୁ ଚିମୁଟାରେ ଧରି ଅନ୍ୟ ପାର୍ଶ୍ଵକୁ ବର୍ଣ୍ଣର (Burner) କିମ୍ବା ସ୍ପିରିଟ୍ ଲ୍ୟାମ୍ପ୍ରେ ଜଳାଇ ପାଉଁଶକୁ ଏକ ୱାବ୍ଗ୍ଲାସ୍ରେ ସଂଗ୍ରହ କରାଯାଉ । ଆଖୁର ସୁରକ୍ଷା ପାଇଁ ଚଷମା ପିନ୍ଧି ଆଖ୍ୟାଠାରୁ ଯଥାସମ୍ଭବ ଦୂରରେ ରଖ୍ ମ୍ୟାଗ୍ନେସିୟମ୍ ପାତକୁ ଜଳାଯାଉ ।
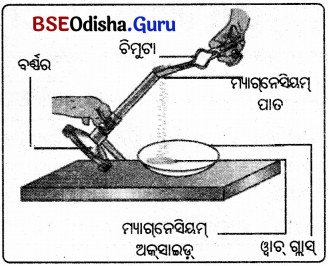
ପର୍ଯ୍ୟବେକ୍ଷଣ : ମ୍ୟାଗ୍ନେସିୟମ୍ ପାତଟି ଅତି ଉଜ୍ଜ୍ବଳ ଧଳାଶିଖା ପ୍ରଦାନ କରି ଜଳିଉଠିବ । ଏହାଫଳରେ କିଛି ଧଳା
ଚୂର୍ଣ୍ଣ ସୃଷ୍ଟି ହେବ । ଏହି ଧଳା ଚୂର୍ଣ୍ଣ ହେଉଛି ମ୍ୟାଗ୍ନେସିୟମ ଅକ୍ସାଇଡ୍ ।
ସିଦ୍ଧାନ୍ତ : ମ୍ୟାଗ୍ନେସିୟମ ଓ ବାୟୁରେ ଥିବା ଅକ୍ସିଜେନ ମଧ୍ୟରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ମ୍ୟାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ୍
ସୃଷ୍ଟି ହୋଇଛି । ଏହା ଏକ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ।
ମ୍ୟାଗ୍ନେସିୟମ + ଅକ୍ସିଜେନ → ମ୍ୟାଗ୍ନେସିୟମ ଅକ୍ସାଇଡ
2Mg + 02 → 2MgO
କର୍ଯ୍ୟାବଳୀ-2 (Activity-2)
ଏକ ପରୀକ୍ଷାନଳୀରେ କିଛି ଲେଡ୍ନାଇଟ୍ରେଟ୍ର ଜଳୀୟଦ୍ରବଣ ନିଆଯାଉ ।
ସେଥ୍ରେ ପୋଟାସିୟମ୍ ଆୟୋଡାଇଡ୍ର ଜଳୀୟଦ୍ରବଣ ମିଶାଯାଉ ।
ପର୍ଯ୍ୟବେକ୍ଷଣ : ଲେଡ୍ ନାଇଟ୍ରେଟ୍ (Pb (NO3)2) ର ଜଳୀୟଦ୍ରବଣ ପୋଟାସିୟମ୍ ଆୟୋଡାଇଡ୍ (KI) ର ଜଳୀୟ ଦ୍ରବଣ ସହ ମିଶିଲେ ଏଥରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ଏକ ଯୌଗିକ ସୃଷ୍ଟି ହେବ ।
ସିଦ୍ଧାନ୍ତ : : ଉତ୍ପନ୍ନ ଯୌଗିକର ନାମ ପୋଟାସିୟମ ନାଇଟ୍ରେଟ୍ (KNO3) ଓ ଲେଡ୍ ଆୟୋଡାଇଡ୍ (PbI2)
ଲେଡ୍ ନାଇଟ୍ରେଟ୍ + ପୋଟାସିୟମ୍ ଆୟୋଡାଇଡ୍ → ପୋଟାସିୟମ୍ ନାଇଟ୍ରେଟ୍ + ଲେଡ୍ ଆୟୋଡାଇଡ୍
Pb(NO3)2 + KI → 2KNO3 + Pb2,
![]()
କର୍ଯ୍ୟାବଳୀ-3 (Activity-3)
ଏକ କୋନିକାଲ୍ ଫ୍ଲାସ୍ କିମ୍ବା ଏକ ପରୀକ୍ଷା
ନଳୀରେ କିଛି ଜିନା ନିଆଯାଉ ।
ସେଥିରେ କିଛି ଲଘୁ ହାଇଡ୍ରୋକ୍ଲୋରିକ୍ ଏସିଡ୍
କିମ୍ବା ସଫ୍ୟୁରିକ୍ ଏସିଡ୍ ମିଶାଯାଉ ।
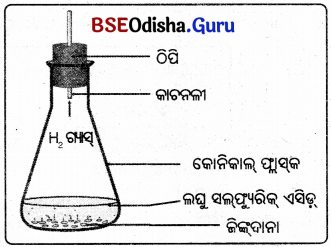
ପର୍ଯ୍ୟବେକ୍ଷଣ : ଏକ କୋନିକାଲ ଫ୍ଲାସ୍ କିମ୍ବା
ପରୀକ୍ଷାନଳୀରେ କିଛି ଜିନା ସହିତ ଲଘୁ ଗନ୍ଧକାମ୍ଳ ବା ଲଘୁ ଲବଣାମ୍ଳ ମିଶାଇଲେ ସଙ୍ଗେ ସଙ୍ଗେ ପରୀକ୍ଷା ନଳୀଟି ତାତି ଯିବ ଏବଂ ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ନିର୍ଗତ ହେବ ।
ସିଦ୍ଧାନ୍ତ : ଜିଙ୍କ୍ ଦାନା ସହିତ ଲଘୁ ଗନ୍ଧକାମ୍ଳ ବା ଲଘୁ ଲବଣାସ୍କର ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ଜିଙ୍କ୍ ସଲଫେଟ୍ (ZnSO4) ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ସୃଷ୍ଟି ହୋଇଥାଏ |
ଜିଙ୍କ୍ + ଲଘୁ ସଫ୍ୟୁରିକ ଏସିଡ୍ → ଜିଙ୍କ୍ ସଲଫେଟ୍ + ହାଇଡ୍ରୋଜେନ୍ (↑)
Zn + H2SO4 → ZnSO4 + H2↑
କାର୍ଯ୍ୟାବଳୀ -4 (Activity-4)
ଅକ୍ ପରମ।ଣର କଥାକସିସ୍ମ ଅକ୍ସାଇଡ୍
କିମ୍ବା କଲିଚୂନ (Quick lime) ଏକ ବିକର୍ରେ ନିଆଯାଉ ।
ଏଥିରେ ଧୀରେ ଧୀରେ ଜଳ ମିଶାଯାଉ ।
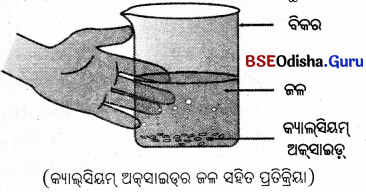
ପର୍ଯ୍ୟବେକ୍ଷଣ :
କ୍ୟାଲସିୟମ୍ ଅକସାଇଡ୍ ବା କଲିଚୂନର ଜଳ ସହିତ ପ୍ରତିକ୍ରିୟା ଘଟି ପ୍ରଚୁର ପରିମାଣର ତାପ ନିର୍ଗତ ହେବା ସଙ୍ଗେ ସଙ୍ଗେ ଶର୍ମିତ ଚୂନ (Slaked lime) ଉତ୍ପନ୍ନ ହୁଏ ।

ବିକରଟିକୁ ଛୁଇଁଲେ ଜଣାଯିବ ଯେ, ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ପ୍ରଚୁର ପରିମାଣର ତାପ ସୃଷ୍ଟି ହେଉଛି ।
ସିଦ୍ଧାନ୍ତ :
ଉପରୋକ୍ତ ପ୍ରତିକ୍ରିୟାରେ କ୍ୟାଲ୍ସିୟମ୍ ଅକ୍ସାଇଡ୍ (CaO) ଓ ଜଳ (H2O) ସଂଯୁକ୍ତ ହୋଇ ଏକମାତ୍ର ଉତ୍ପାଦ କ୍ୟାଲସିୟମ୍ ହାଇଡ୍ରିକ୍ସାଇଡ୍ (Ca(OH)2)ଉତ୍ପନ୍ନ ହୋଇଛି । ଏହା ଏକ ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟା । ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାକୁ ନିମ୍ନମତେ ପ୍ରକାଶ କରାଯାଏ ।

ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାରେ ପ୍ରତିକାରକଗୁଡ଼ିକର ପରମାଣୁଗୁଡ଼ିକ ମଧ୍ୟରେ ଥିବା ରାସାୟନିକ ବନ୍ଧଗୁଡ଼ିକ ଭାଙ୍ଗିଯାଏ ଏବଂ ନୂତନ ରାସାୟନିକ ବନ୍ଧ ଗଠିତ ହୁଏ । ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାର ଭିନ୍ନ ଉଦାହରଣଗୁଡ଼ିକୁ ଲକ୍ଷ୍ୟକର : ସଂଶ୍ଳେଷଣ ପ୍ରତିକ୍ରିୟାର ଅନ୍ୟ କେତେକ ଉଦାହରଣ ନିମ୍ନରେ ଦିଆଯାଇଛି :
(i) କୋଇଲାର ଦହନରୁ ଅଙ୍ଗାରକାମ୍ଳ ଗ୍ୟାସ୍ ସୃଷ୍ଟି ହୋଇଥାଏ ।
C(s) + 02(g) → CO2(g)
(ii) ହାଇଡ୍ରୋଜେନ୍ ଓ ଅକ୍ସିଜେନ୍ ସଂଯୋଗରୁ ଜଳ ସୃଷ୍ଟି ହୋଇଥାଏ ।
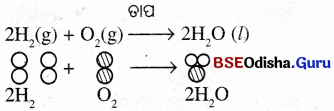
କାର୍ଯ୍ୟାବଳୀ -5 (Activity-5)
ଏକ ଶୁଷ୍କ ସ୍ଫୁଟନ ନଳୀ (Boiling tube) ରେ ପ୍ରାୟ 2 ଗ୍ରାମ୍ ଫେରସ୍ ସଲ୍ଫେଟ୍ ସ୍ଫଟିକ (Crystal) ନିଆଯାଉ ।
ସ୍ଫଟିକ ନଳୀକୁ ବର୍ଣ୍ଣର୍ ବା ସ୍ପିରିଟ୍ ଲ୍ୟାମ୍ପ୍ରେ ଗରମ କରାଯାଉ ।
ଫେରସ୍ ସଲ୍ଫେଟ୍ ସ୍ଫଟିକର ରଙ୍ଗକୁ ଲକ୍ଷ୍ୟ
ପର୍ଯ୍ୟବେକ୍ଷଣ: ଫେରସ୍ ସଲ୍ଫେଟ୍ ସ୍ଫଟିକ
(FeSO4, 7H2O) ଉତ୍ତପ୍ତ ହେଲେ ଏହା
ରଙ୍ଗକୁ ବଦଳିଯାଇଥାଏ ।

ସିଦ୍ଧାନ୍ତ:
ଫେରସ୍ ସଲ୍ଫେଟ୍ ସ୍ଫଟିକ ବିଘଟିତ ହୋଇ ଫେରିକ୍ ଅକ୍ସାଇଡ୍ (Fe2O3), ସଲଫର ଡାଇଅକ୍ସାଇଡ (SO2) ଏବଂ ସଲଫର ଟ୍ରାଇଅକ୍ସାଇଡ (SO3)ରେ ପରିଣତ ହୁଏ ।
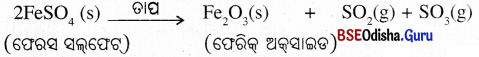
କାର୍ଯ୍ୟାବଳୀ -6 (Activity-6)
ଏକ ସ୍ଫୁଟନ ନଳୀରେ ପ୍ରାୟ 2 ଗ୍ରାମ୍ ଲେଡ୍ନାଇଟ୍ରେଟ୍ ଚୂର୍ଣ୍ଣ ନିଆଯାଉ ।
ସ୍ଫୁଟନ ନଳୀଟିକୁ ଏକ ଚିମୁଟା (Tongs)ରେ ଧରି ଗରମ କରାଯାଉ ।
ପର୍ଯ୍ୟବେକ୍ଷଣ:
ନଳୀର ଗରମ ଫଳରେ ବାଦାମୀ ରଙ୍ଗର ଧୂମ ଉତ୍ସର୍ଜନ (cmission) ହେବ । ଏହି ଧୂମ ହେଉଛି ନାଇଟ୍ରୋଜେନ୍ ଡାଇଅକ୍ସାଜି (NO2) |

ସିଦ୍ଧାନ୍ତ:
ଲେଡ୍ ନାଇଟ୍ରେଟ୍ ଚୂର୍ଣ ବିଘଟିତ ହୋଇ ଲେଡ୍ ଅକ୍ସାଇଡ୍, ନାଇଟ୍ରୋଜୋନ୍ ଡାଇଅକ୍ସାଇଡ୍ ଓ ଅକ୍ସିଜେନ୍ ଗ୍ୟାସ୍ରେ ପରିଣତ ହୋଇଥାଏ ।

ଅନ୍ୟ କେତେକ ରତ୍ନାତୂତଣ:
(i) ସିଲ୍ଭର କ୍ଲୋରାଇଡ୍ ସୂର୍ଯ୍ୟାଲୋକରେ ବିଘଟନ ହୋଇ ସିଲ୍ଭର ଓ କ୍ଲୋରିନ୍ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ ହୋଇଥାଏ ।
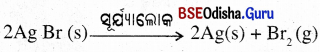
(ii) ସିଲ୍ଭର ବ୍ରୋମାଇଡ୍ ସୂର୍ଯ୍ୟାଲୋକ ଉପସ୍ଥିତିରେ ବିଘଟନ ହୋଇ ସିଲ୍ଭର୍ ଓ ବ୍ରୋମିନ୍ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ ହୋଇଥାଏ ।
![]()
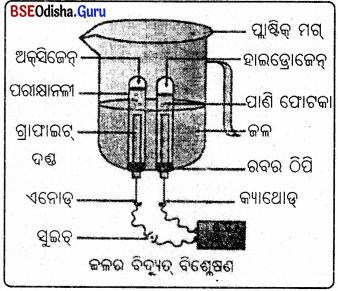
କାର୍ଯ୍ୟାବଳୀ -7 (Activity-7)
(i) ଗୋଟିଏ ପ୍ଲାଷ୍ଟିକ୍ ମର୍ ନେଇ ଏହାର ତଳପଟରେ ଦୁଇଟି କଣା କରାଯାଉ । କଣାଥିବା ଦୁଇଟି ରବର ଠିପି ଏଥରେ ଲଗାଯାଉ । ଚିତ୍ରରେ ଦର୍ଶାଯାଇଥିବା ଭଳି କାର୍ବନ ଇଲେକ୍ଟ୍ରୋଡ୍ ଦୁଇଟିକୁ ଏହି ରବର
(ii) ଏହି ଇଲେକ୍ଟ୍ରୋଡ୍ ଦୁଇଟିକୁ ଗୋଟିଏ 6 ଭୋଲ୍ଟ ବ୍ୟାଟେରୀ ସହିତ ସଂଯୋଗ କରାଯାଉ ।
(iii) ମଲ୍ଟିଟିରେ ଜଳ ଭର୍ତ୍ତି କରାଯାଉ ଯେପରିକି ବୁନ୍ଦା ଲଘୁ ସଲ୍ଫ୍ୟୁରିକ୍ ଏସିଡ଼୍ ଜଳରେ ମିଶାଯାଉ ।
(iv) ଜଳପୂର୍ଣ୍ଣ ଦୁଇଟି ପରୀକ୍ଷାନଳୀ ନେଇ ସେଗୁଡ଼ିକୁ କାର୍ବନ ଇଲେକ୍ଟ୍ରୋଡ଼ ଦୁଇଟି ଉପରେ ଓଲଟା ରଖାଯାଉ ।
(v) ସୁଇଚ୍ ଟିପି ଉପକରଣ ମଧ୍ୟକୁ ବିଦ୍ୟୁତ୍ ପ୍ରବାହ କରାଯାଉ । .
ପର୍ଯ୍ୟବେକ୍ଷଣ :
(i) କିଛି ସମୟ ପରେ ଲକ୍ଷ୍ୟକଲେ ଦେଖାଯିବ ଯେ, ଉଭୟ ଇଲେକ୍ଟ୍ରୋଡ଼ଠାରେ ପାଣି ଫୋଟକା ସୃଷ୍ଟି ହେଉଛି ।
(ii) ପରୀକ୍ଷାନଳୀ ଦୁଇଟି ଗ୍ୟାସ୍ ପୂର୍ଣ ହୋଇଗଲା ପରେ ସତର୍କତାର ସହ ସେହି ଦୁଇଟିକୁ କାଢ଼ି ନିଆଯାଉ ।
(iii) ଏକ ଜଳନ୍ତା ମହମବତୀକୁ ପରୀକ୍ଷାନଳୀର ମୁହଁ ପାଖକୁ ଆଣି ଦେଖାଇଲେ ଗୋଟିଏ ପରୀକ୍ଷାନଳୀରେ ଥିବା ଗ୍ୟାସ୍ ପପ୍ ଶବ୍ଦ କରି ଜଳିବ ଏବଂ ଅନ୍ୟଟିରେ କାଠିଟି ଅତି ଉଜ୍ଜଳ ଭାବରେ ଜଳିବ । ଯେଉଁ ଗ୍ୟାସ୍ଟ୍ରି ପପ୍ ଶବ୍ଦ କରି ଜଳିଯିବ ତାହା ଉଦ୍ଜାନ ଏବଂ ଉଜ୍ଜ୍ଵଳ ଭାବେ ଜଳୁଥିବା ଗ୍ୟାସ୍ ଅମ୍ଳଜାନ ।
ସିଦ୍ଧାନ୍ତ :
ଜଳରୁ ବିଦ୍ୟୁତ୍ ବିଶ୍ଳେଷଣ କଲେ ସେଥୁରୁ ଉଦ୍ଜାନ ଓ ଅମ୍ଳଜାନ ଗ୍ୟାସ୍ ନିର୍ଗତ ହୁଏ, ଯେତିକି ଅମ୍ଳଜାନ ଗ୍ୟାସ୍ ନିର୍ଗତ ହୁଏ, ତାହାର ଆୟତନର ଦୁଇଗୁଣ ଉଦ୍ଜାନ ଗ୍ୟାସ୍ ନିର୍ଗତ ହୁଏ । ବିଘଟନ ପ୍ରତିକ୍ରିୟା ମାଧ୍ୟମରେ ଜଳରେ ବୈଦ୍ୟୁତିକ ବିଶ୍ଳେଷଣ୍ଢ ସମ୍ଭବ ।
ଉଦାହରଣ:
(i) ତରଳ ଆଲୁମିନା ମଧ୍ୟ ଦେଇ ବିଦ୍ୟୁତ୍ ସ୍ରୋତ ପ୍ରବାହିତ କଲେ ତାହା ବିଘଟିତ ହୋଇ ଆଲୁମିନିୟମ୍ ଓ ଅମ୍ଳଜାନ ମିଳିଥାଏ । ଏହା ଆଲୁମିନିୟମ୍ ଉତ୍ପାଦନର ଔଦ୍ୟୋଗିକ ପଦ୍ଧତି ଅଟେ ।
![]()
(ii) ତରଳ ଆଲୁମିନା ମଧ୍ୟ ଦେଇ ବିଦ୍ୟୁତ୍ ସ୍ରୋତ ପ୍ରବାହିତ କଲେ ତାହା ବିଘଟିତ ହୋଇ ଆଲୁମିନିୟମ୍ ଓ ଅମ୍ଳଜାନ ମିଳିଥାଏ । ଏହା ଆଲୁମିନିୟମ୍ ଉତ୍ପାଦନର ଔଦ୍ୟୋଗିକ ପଦ୍ଧତି ଅଟେ ।
କ୍ଲୋରିନ୍ ମିଳିଥାଏ । ଏହା ମଧ୍ୟ ଏକ ଔଦ୍ୟୋଗିକ ପଦ୍ଧତି ଅଟେ ।
![]()
(iii) ଅମ୍ଳୀକୃତ ଜଳ ମଧ୍ୟରେ ବିଦ୍ୟୁତ୍ ପ୍ରବାହ କଲେ ଜଳ ଉଦ୍ଜାନ ଓ ଅମ୍ଳଜାନକୁ ବିଘଟିତ ହୋଇଥାଏ ।
![]()
କାର୍ଯ୍ୟାବଳୀ -8 (Activity-8)
(i) ଏକ ଚିନାମାଟି ଥାଳିଆରେ ପ୍ରାୟ 2 ଗ୍ରାମ୍ ସିଲଭର୍ କ୍ଲୋରାଇଡ୍ ନିଆଯାଉ ।
(ii) ଏହି ଚିନାମାଟି ଥାଳିଆକୁ କିଛି ସମୟ ପାଇଁ ସୂର୍ଯ୍ୟାଲୋକରେ ରଖାଯାଉ ।
ପର୍ଯ୍ୟବେକ୍ଷଣ :
(i) କିଛି ସମୟ ପରେ ଦେଖାଯିବ ଯେ, ସିଲ୍ଭର୍ କ୍ଲୋରାଇଡ଼ ସୂର୍ଯ୍ୟାଲୋକ ଉପସ୍ଥିତିରେ ଧଳାରଙ୍ଗରୁ ଧୂସର ରଙ୍ଗରେ ପରିଣତ ହୋଇଛି ।
(ii) ସୂର୍ଯ୍ୟାଲୋକରେ ସିଲ୍ଭର କ୍ଲୋରାଇଡ୍ର ବିଘଟନ ଘଟି ସିଲ୍ଭର୍ ଓ କ୍ଲୋରିନ୍ ଉତ୍ପନ୍ନ ହେଉଥିବା ଯୋଗୁଁ ଏପରି ହୋଇଛି ।
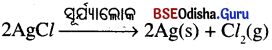
ସିଦ୍ଧାନ୍ତ :
ବିଘଟନ ପ୍ରତିକ୍ରିୟାଗୁଡ଼ିକ ପ୍ରତିକାରକଗୁଡ଼ିକର ବିଘଟନ ପାଇଁ ତାପ, ଆଲୋକ କିମ୍ବା ବିଦ୍ୟୁତ୍ ଶକ୍ତି ଆବଶ୍ୟକ କରିଥା’ନ୍ତି ।
ଉଦାହରଣ:
(i) ଆଲୋକ ଉପସ୍ଥିତିରେ ହାଇଡ୍ରୋଜେନ୍ ପେରକ୍ସାଇଡ଼ ବିଘଟିତ ହୋଇ ହାଇଡ୍ରୋଜେନ୍ ଓ ଅମ୍ଳଜାନ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ ହୋଇଥାଏ ।
![]()
(ii) ଆଲୋକ ଉପସ୍ଥିତିରେ ନାଇଟ୍ରିକ୍ ଅମ୍ଳ ବିଘଟିତ ହୋଇ ଜଳ, ନାଇଟ୍ରୋଜେନ୍ ଡାଇଅକ୍ସାଇଡ୍ ଓ ଅମ୍ଳଜାନ ଗ୍ୟାସ୍ ମିଳିଥାଏ ।
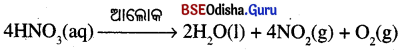
କାର୍ଯ୍ୟାବଳୀ -9 (Activity-9)
(i) ତିନୋଟି ଲୁହା କଣ୍ଟା ନେଇ ସେଗୁଡ଼ିକୁ ବାଲିକାଗଜରେ ଘସି ସଫା କରାଯାଉ ।
(ii) A ଓ B ଚିହ୍ନିତ କରି ଦୁଇଟି ପରୀକ୍ଷାନଳୀ ନିଆଯାଉ । ପ୍ରତ୍ୟେକ ପରୀକ୍ଷାନଳୀରେ ପ୍ରାୟ 10 ମିଲିଲିଟର କପର ସଲ୍ଫେଟ୍ ଦ୍ରବଣ ନିଆଯାଉ ।
(iii) ଖଣ୍ଡିଏ ସୂତାରେ କଣ୍ଟା ଦୁଇଟିକୁ ବାନ୍ଧି ସାବଧାନତା ସହ ପରୀକ୍ଷାନଳୀରେ ଥିବା କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣରେ ପ୍ରାୟ 20 ମିନିଟ୍ ପାଇଁ ବୁଡ଼ାଇ ରଖାଯାଉ । ତୁଳନା କରିବା ନିମନ୍ତେ ଗୋଟିଏ ଲୁହାକଣ୍ଟା ଅଲ ଗା ରଖାଯାଉ ।
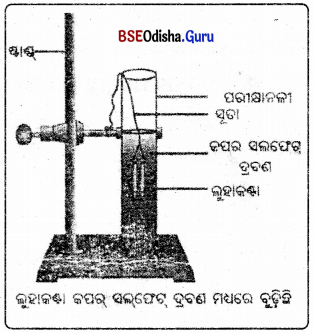
(iv) 20 ମିନିଟ୍ ପରେ ଲୁହାକଣ୍ଟା ଦୁଇଟିକୁ କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣରୁ ବାହାର କରି ଆଣି ପରୀକ୍ଷାନଳୀ A ଓ Bରେ ଥିବା କପର ସଲ୍ଫେଟ୍ ଦ୍ରବଣର ନୀଳରଙ୍ଗର ତୀବ୍ରତା ସହିତ ତୁଳନା କରାଯାଉ ।
(v) କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣରେ ବୁଡ଼ାଯାଇଥିବା ଲୁହାକଣ୍ଟା ଦୁଇଟିର ରଙ୍ଗକୁ ଅଲଗା ରଖାଯାଇଥିବା ଲୁହାକଣ୍ଟାର ରଙ୍ଗ ସହିତ ମଧ୍ୟ ତୁଳନା କରାଯାଉ ।


ପର୍ଯ୍ୟବେକ୍ଷଣ :
ଲୁହାକଣ୍ଟା ଟିକିଏ ବାଦାମି ରଙ୍ଗ ଧାରଣ କରିଛି ଏବଂ କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣର ନୀଳରଙ୍ଗର ତୀବ୍ରତର ହ୍ରାସ ଘଟିଛି । କାରଣ ଲୌହ କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣରୁ କପର୍କୁ ବିସ୍ଥାପିତ କରିଛି । ଏଠାରେ ଲୌହ କପଠାରୁ ଅଧିକ କ୍ରିୟାଶୀଳ ଧାତୁ ।
ସିଦ୍ଧାନ୍ତ :
ଏହି ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଆଇରନ୍ (Fe) ଅନ୍ୟ ମୌଳିକ କପର୍ (Cu)କୁ କପର୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣରୁ ଅପସାରଣ ବା ବିସ୍ଥାପନ କରିଛି । ଏହି ପ୍ରତିକ୍ରିୟାକୁ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ ।
![]()
କାର୍ଯ୍ୟାବଳୀ -10 (Activity-10)
ଏକ ପରୀକ୍ଷାନଳୀରେ ପ୍ରାୟ 3 ମିଲି ଲି. ସୋଡ଼ିୟମ୍ ସଲ୍ଫେଟ୍ ଦ୍ରବଣ ନିଆଯାଉ ।
ଅନ୍ୟ ଏକ ପରୀକ୍ଷା ନଳୀରେ ପ୍ରାୟ 3 .ମିଲି ଲି. ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ ଦ୍ରବଣ ନିଆଯାଉ ।
ଦୁଇଟି ଦ୍ରବଣକୁ ମିଶାଇ ଦିଆଯାଉ ।
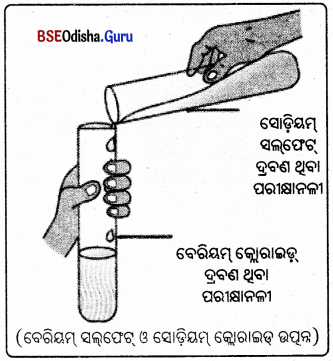
ପର୍ଯ୍ୟବେକ୍ଷଣ :
ବେରିୟମ୍ କ୍ଲୋରାଇଡ଼ ଦ୍ରବଣ ସହିତ ମିଶାଇଲେ, ଉକ୍ତ ମିଶ୍ରଣ ଫଳରେ ଏକ ଧଳା ପଦାର୍ଥ ସୃଷ୍ଟି ହୋଇଥାଏ । ଯାହା ଜଳରେ ଦ୍ରବଣୀୟ ନୁହେଁ । ଉତ୍ପନ୍ନ ଅଦ୍ରବଣୀୟ ପଦାର୍ଥକୁ ଅବକ୍ଷେପ କହନ୍ତି । ହେଉଥିବା ଏହି
ଯେଉଁ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଅବକ୍ଷେପ ସୃଷ୍ଟି ହୁଏ, ତାକୁ ଅବକ୍ଷେପଣ ପ୍ରତିକ୍ରିୟା (Precipitation reaction) କହନ୍ତି । ସୋଡ଼ିୟମ୍ ସଲଫେଟ୍ ଓ ବେରିୟମ୍ କ୍ଲୋରାଇଡ୍ ମଧ୍ୟରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ବେରିୟମ ସଲଫେଟ୍ (ଅଦ୍ରବଣୀୟ ଧଳା ଅବକ୍ଷେପ) ଓ ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ (ଜଳରେ ଦ୍ରବଣୀୟ) ସୃଷ୍ଟି ହୋଇଥାଏ । ଏ କ୍ଷେତ୍ରରେ SO42- ଓ Ba2+ ମଧ୍ୟରେ ପ୍ରତିକ୍ରିୟା ହେତୁ ଅଦ୍ରବଣୀୟ ଧଳା ଅବକ୍ଷେପ BaSO4, ଉତ୍ପନ୍ନ ହୁଏ ଏବଂ ଅନ୍ୟ ଉତ୍ପାଦଟି Na+ ଓ CI– ର ପ୍ରତିକ୍ରିୟା ହେତୁ ସୋଡ଼ିୟମ କ୍ଲୋରାଇଡ ଉତ୍ପନ୍ନ ହୋଇଥାଏ, ଯାହା ଦ୍ରବଣ ମଧ୍ୟରେ ରହିଯାଏ ।
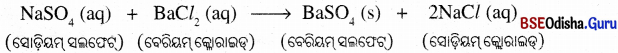
ସିଦ୍ଧାନ୍ତ :
SO42- ଓ Ba2+ ମଧ୍ୟରେ ପ୍ରତିକ୍ରିୟା ଯୋଗୁଁ ଧଳା ଅବକ୍ଷେପ BaSO4, ଉତ୍ପନ୍ନ ହୋଇଛି । ଅନ୍ୟ ଉତ୍ପାଦ ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ଼ ଜଳରେ ଦ୍ରବଣୀୟ । ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ପ୍ରତିକାରକ ଦୁଇଟି ମଧ୍ୟରେ ଆୟନ ବିନିମୟ ଘଟିଥାଏ । ତେଣୁ ଏହା ଏକ ଦୈତ୍ୟ ବିସ୍ଥାପିତ ପ୍ରତିକ୍ରିୟା ଅଟେ ।
ଉଦାହରଣ:
ଲେଡ୍ ନାଇଟ୍ରେଟ୍ ଦ୍ରବଣ ସହିତ ପୋଟାସିୟମ୍ ଆୟୋଡ଼ାଇଡ୍ ଦ୍ରବଣ ମିଶାଇଲେ ଲେଡ୍ ଆୟୋଡ଼ାଇଡ୍ ଓ ପୋଟାସିୟମ୍ ନାଇଟ୍ରେଟ୍ ଦ୍ରବଣ ଉତ୍ପନ୍ନ ହେବ ।
Pb (NO3)2 + KI → PbI2, + KNO3 ଏହା ଏକ ଦ୍ଵୈତ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା ଅଟେ ।
କାର୍ଯ୍ୟାବଳୀ -11 (Activity-11)
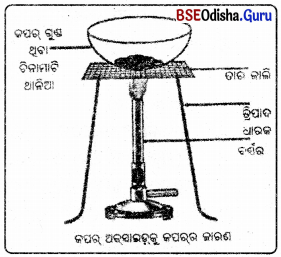
(i) ଏକ ଚିନାମାଟି ଥାଳିଆରେ ପ୍ରାୟ l ଗ୍ରାମ୍ କପର ଗୁଣ୍ଡ ନେଇ ଗରମ କରାଯାଉ ।
(ii) କପର୍ ଗୁଣ୍ଡର ଚାରିପଟେ କପର୍ (II) ଅକ୍ସାଇଡ୍ର ଏକ କଳା ଆସ୍ତରଣ ସୃଷ୍ଟି ହେବ ।
(iii) ଏହି କଳା ଆସ୍ତରଣ ହେଉଛି କପର୍ ଅକ୍ ସାଇଡ଼ । ଅକ୍ସିଜେନ୍ର କପର୍ ସହିତ ସଂଯୋଗ ଘଟି କପର୍ ଅକ୍ସାଇଡ୍ ଉତ୍ପନ୍ନ ହୋଇଛି ।
![]()
(iv) ଯଦି ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍କୁ ଏହି ଉତ୍ତପ୍ତ ପଦାର୍ଥ (CuO) ଉପରେ ପ୍ରବାହିତ କରାଯାଏ, ତେବେ ବିପରୀତ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି କଳା ଆସ୍ତରଣଟି ବାଦାମୀ ରଙ୍ଗରେ ପରିଣତ ହୁଏ ଓ କପର୍ ମିଳିଥାଏ ।
![]()
ସିଦ୍ଧାନ୍ତ :
(i)ଯଦି ଏକ ପଦାର୍ଥ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମୟରେ ଅକ୍ସିଜେନ୍ ଲାଭ କରେ, ତେବେ ପଦାର୍ଥଟି ଜାରିତ (Oxidised) ହେଲା ବୋଲି କୁହାଯିବ । କିନ୍ତୁ ଯଦି ପଦାର୍ଥଟି ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମୟରେ ଅକ୍ସିଜେନ୍ ହରାଇଥାଏ, ତେବେ ତାହା ବିଜାରିତ (Reduced) ହେଲା ବୋଲି କୁହାଯିବ ।
(ii) ଏହି ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସମୟରେ କପର୍ (II) ଅକ୍ସାଇଡ୍ ଅକ୍ସିଜେନ୍ ହରାଉଛି ଏବଂ ବିଜାରିତ ହେଉଛି । ହାଇଡ୍ରୋଜେନ୍ ଅକ୍ସିଜେନ୍ ଲାଭ କରୁଛି ଏବଂ ଜାରିତ ହେଉଛି । ଏହା ଜାରଣ-ବିଜାରଣ ପ୍ରତିକ୍ରିୟାର ଅନ୍ତର୍ଗତ ।
