Odisha State Board BSE Odisha 10th Class Physical Science Notes Chapter 3 ଧାତୁ ଓ ଅଧାତୁ will enable students to study smartly.
BSE Odisha Class 10 Physical Science Notes Chapter 3 ଧାତୁ ଓ ଅଧାତୁ
→ ଉପକ୍ରମ (Introduction):
- ଆଜି ପର୍ଯ୍ୟନ୍ତ ଆବିଷ୍କୃତ 118ଟି ମୌଳିକ ମଧ୍ୟରୁ କେତେକ ପ୍ରାକୃତିକ ଓ କେତକ କୃତ୍ରିମ ମୌଳିକ ଅଟନ୍ତି । ପ୍ରାକୃତିକ ମୌଳିକମାନଙ୍କୁ ଧାତୁ, ଅଧାତୁ କିମ୍ବା
- ଉପଧାତୁ ରୂପେ ଶ୍ରେଣୀଭୁକ୍ତ କରାଯାଇଛି ।
- ଲୁହା, ତମ୍ବା, ଏଲୁମିନିୟମ୍, ସୋଡ଼ିୟମ୍, ଜିଙ୍କ୍ ଇତ୍ୟାଦି ସହଜରେ ମିଳୁଥିବା ଧାତୁ (Metal) ଅଟନ୍ତି ।
- କେତେକ ଧାତୁକୁ ବିଭିନ୍ନ ଉପକରଣ ଭାବରେ ଓ କେତେକକୁ ଅଳଙ୍କାର ରୂପେ ବ୍ୟବହାର କରାଯାଏ ।
- କାର୍ବନ, ସଲଫର୍, ଫସଫରସ, ଅମ୍ଳଜାନ, ଉଦ୍ଜାନ ଇତ୍ୟାଦି ସହଜରେ ମିଳୁଥିବା ଅଧାତୁ (Non-Metal) ଅଟନ୍ତି ।
- ଏମାନଙ୍କୁ ବିଭିନ୍ନ ବ୍ୟବହାର୍ଯ୍ୟ ପଦାର୍ଥ ରୂପେ ବ୍ୟବହାର କରାଯାଏ ।
- କେତେକ ମୌଳିକ ଯେଉଁମାନେ ଉଭୟ ଧାତୁ ଓ ଅଧାତୁର ଗୁଣ ପ୍ରଦର୍ଶନ କରନ୍ତି, ସେଗୁଡ଼ିକୁ ଉପଧାତୁ (Metalloids) କହନ୍ତି । ବୋରନ୍, ସିଲିକନ୍, ଜର୍ମାନିୟମ୍ , ଆର୍ସେନିକ୍, ଏକ୍ସିମନି, ଟେଲୁରିୟମ୍, ପୋଲୋନିୟମ୍ ଆଦି ଉପଧାତୁ ଅଟନ୍ତି ।
→ ଧାତ୍ରଶ୍ନଡ଼ିକର ଭୌତିକ ଧର୍ମ (Physical properties of metals):
→ ଅଧାତୁଗୁଡ଼ିକର ଭୌତିକ ଶ୍ରଣ (Physical properties of non-metals):
- ଅଧାତୁଗୁଡ଼ିକ ଅନମନୀୟ ଓ ଭଙ୍ଗୁର ଅଟନ୍ତି । କଠିନ ଅଧାତୁକୁ ହାମରରେ ପିଟି ଚଦରପରି କରାଯାଇପାରିବ ନାହିଁ । ନାହିଁ ।
- ଅଧାତୁଗୁଡ଼ିକ ତନ୍ୟ ନୁହଁନ୍ତି । କଠିନ ଅଧାତୁରୁ ଆମେ ତାର ତିଆରି କରିପାରିବା ନାହିଁ ।
- ଅଧାତୁଗୁଡ଼ିକ ତାପ ଓ ବିଦ୍ୟୁତ୍ କୁପରିବାହୀ ।
- ଅଧାତୁଗୁଡ଼ିକର ମୁକ୍ତ ଇଲେକ୍ଟ୍ରନ ନ ଥିବାରୁ ସେଗୁଡ଼ିକ ବିଦ୍ୟୁତ୍ ପରିବହନ କରନ୍ତି ନାହିଁ ।
- ଅଧାତୁଗୁଡ଼ିକର ଧାତବ ଔଜଲ୍ୟ ବା ଦୀପ୍ତି ନାହିଁ । (ଆୟୋଡ଼ିନ୍ ଓ ଗ୍ରାଫାଇଟ୍ ବ୍ୟତୀତ)
→ ଅଧାତୁର ରାସାପାନିଜ ଶ୍ରଣ (Chemical properties of non-metals):
→ ଧାତୁର ରାସାୟନିକ ଧର୍ମ (Chemical properties of metals):
![]()
(a) ଧାତୁକୁ ରାଷ୍ଟ ସହିତ ବଦନ (Metals burnt with Air):
- ଧାତୁ ଅମ୍ଳସହ ପ୍ରତିକ୍ରିୟା (Reaction of Metals with Acids):
- ଧାତୁ ଅମ୍ଳସହ ପ୍ରତିକ୍ରିୟା କରି ଲବଣ ଓ ହାଇଡ୍ରୋଜେନ ଗ୍ୟାସ୍ ଉତ୍ପନ୍ନ କରେ ।
ଧାତୁ + ଲଘୁ ଅମ୍ଳ → ଲବଣ + ହାଇଡ୍ରୋଜେନ୍
→ ଧାତୁର ଅନ୍ୟ ଧାତବ ଲବଣର ଦ୍ରବଣ ସହ ପ୍ରତିକ୍ରିୟା (Reaction metals with solutions of other metal salts):
→ ଧାତୁ ଓ ଅଧାତୁ କିପରି ପ୍ରତିକ୍ରିୟା କରେ (How do metals and non-metals react ?):
- ନୋବେଲ୍ ଖ୍ୟାପଗୁଡିକର ଫପୋଜକ କକ୍ଷରେ ସମ୍ପୂର୍ଣ୍ଣ ମାତ୍ରାରେ ଇଲେକ୍ଟ୍ରନ ଥିବାରୁ ସେଗୁଡ଼ିକ ରାସାୟନିକ ସକ୍ରିୟତା ପ୍ରଦର୍ଶନ କରନ୍ତି ନାହିଁ ।
- ଧାତୁ ଗୁଡ଼ିକ ସହଜରେ ଇଲେକ୍ଟ୍ରନ୍ ତ୍ୟାଗକରି ଯୁକ୍ତାତ୍ମକ ଆୟନରେ ପରିଣତ ହୁଅନ୍ତି । ଅଧାତୁ ଗୁଡ଼ିକ ଇଲେକ୍ଟ୍ରନ୍ ଗ୍ରହଣ କରି ବିଯୁକ୍ତାତ୍ମକ ଆୟନ୍ରେ ପରିଣତ ହୁଅନ୍ତି । ଫଳରେ ଧାତୁ ଓ ଅଧାତୁ ନିକଟତମ ନୋବଲ୍ ଗ୍ୟାସ୍ର ଇଲେକ୍ନ ସଂରଚନା ଧାରଣ କରନ୍ତି ।
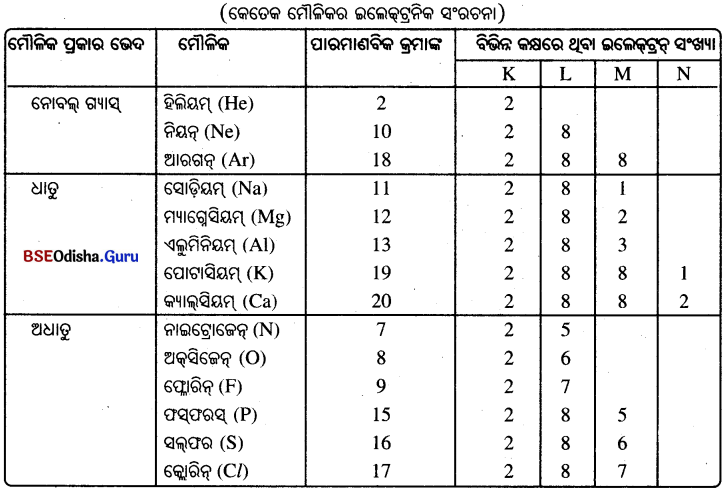
→ ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ (NaCI) ଯୌଗିକର ଗଠନ :
- ସୋଡ଼ିୟମ୍ ପରମାଣୁର ଇଲେକ୍ଟ୍ରନ ସଂରଚନା 2, 8, 1 ।
- ଏହାର M କକ୍ଷରେ ଗୋଟିଏ ଇଲେକ୍ଟ୍ରନ ଅଛି । ଏହା ଯଦି M କକ୍ଷର ଗୋଟିଏ ଇଲେକ୍ଟ୍ରନ୍ ହରାଇ ଦିଏ ତେବେ L କକ୍ଷଟି ବାହ୍ୟତମ କକ୍ଷ ହୋଇଯିବ
- । ଏହା ଏକ ସ୍ଥାୟୀ ଅଷ୍ଟକ ଅଟେ । ଏହାର ପରମାଣୁର ନ୍ୟୁକ୍ଲିୟସରେ 11 ଟି ପ୍ରୋଟନ୍ ରହିଛି ଓ ଇଲେକ୍ଟ୍ରନ ସଂଖ୍ୟା 10 ହୋଇଯାଇଛି । ବଳକା
- ଗୋଟିଏ ଯୁକ୍ତ ଚାର୍ଜ ସୋଡ଼ିୟମ କାଟାୟନ (Nat) ସୃଷ୍ଟିକରେ ।
- କ୍ଲୋରିନ୍ ପରମାଣୁର ଇଲେକ୍ଟ୍ରନ ସଂରଚନା 2, 8, 7 । ଅଷ୍ଟକ ପୂର୍ଣ୍ଣ ହେବା ପାଇଁ ମାତ୍ର ଗୋଟିଏ ଇଲେକ୍ଟ୍ରନର ଆବଶ୍ୟକତା ରହିଛି ।
ଯଦି ସୋଡ଼ିୟମ୍ ସହିତ କ୍ଲୋରିନ୍ର ପ୍ରତିକ୍ରିୟା ହୁଏ, ତେବେ ସୋଡ଼ିୟମ୍ ହରାଇଥିବା ଗୋଟିଏ ଇଲେକ୍ଟ୍ରନ୍ - ଗୋଟିଏ ଇଲେକ୍ଟ୍ରନ୍ ଗ୍ରହଣ କରିବାପରେ କ୍ଲୋରିନ୍ର ପରମାଣୁ ଗୋଟିଏ ବିଯୁକ୍ତାତ୍ମକ ଚାର୍ଜ ହେବ । କାରଣ ଏହାର ନ୍ୟୁକ୍ଲିୟସ୍ରେ 17 ଟି ପ୍ରୋଟନ୍ ଥିବାବେଳେ K, L ଓ M କକ୍ଷରେ ସମୁଦାୟ 18ଟି ଇଲେକ୍ଟ୍ରମ୍ ।
- ଏହା ଆମକୁ କ୍ଲୋରାଇଡ୍ ଆନାୟନ (CI) ଦେଉଛି, ସେଥିପାଇଁ ଉଭୟ ଯୌଗିକ ମଧ୍ୟରେ ଇଲେକ୍ଟ୍ରନ୍ ଆଦାନ ପ୍ରଦାନ ସମ୍ପର୍କ ସ୍ଥାପନ ହୋଇ ପାରିବ ।
କ୍ଲୋରାଇଡ୍ ଆୟନ (CI) ହେବ
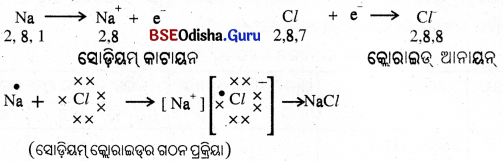
(ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ର ଗଠନ ପ୍ରକ୍ରିୟା) - ସୋଡ଼ିୟମ୍ ଓ କ୍ଲୋରାଇଡ୍ର ଆୟନ ଦ୍ବୟ ବିପରୀତ ଚାର୍ଜ ବିଶିଷ୍ଟ ହୋଇଥିବାରୁ ପରସ୍ପରକୁ ଆକର୍ଷଣ କରେ ଏବଂ ଶକ୍ତିଶାଳୀ ସ୍ଥିର ବିଦ୍ୟୁତ୍ ଆକର୍ଷଣ ବଳଦ୍ଵାରା ଧରିରଖ୍ NaCI ଗଠନ କରେ ।
- ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ ଅଣୁରୂପରେ ନ ରହି ବିପରୀତ ଚାର୍ଜ ଆୟନଗୁଡ଼ିକର ସମଷ୍ଟି ରୂପେ ରହେ ।
ଉଦାହରଣ -2:
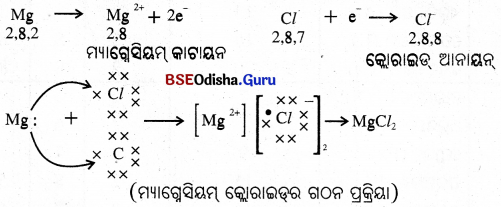
→ ଆୟନିକ ଯୌଗିକ/ବିଦ୍ୟୁତ୍ ସଂଯୋଜ୍ୟ ଯୌଗିକ :
ଧାତୁରୁ ଅଧାତୁକୁ ଇଲେକ୍ଟ୍ରନ୍ର ସ୍ଥାନାନ୍ତରଣ ଦ୍ବାରା ସୃଷ୍ଟି ହେଉଥିବା ଯୌଗିକକୁ ଆୟନିକ ଯୌଗିକ ବା ବିଦ୍ୟୁତ୍ ସଂଯୋଜ୍ୟ (Electrovalent) ଯୌଗିକ କୁହାଯାଏ ।
→ ଆୟନିକ ଯୌଗିକର ଧର୍ମ (Properties of lonic Compounds):
→ ଧାତୁର ଉପସ୍ଥିତି (Occurrence of Metals) :
- ଧାତୁର ମୁଖ୍ୟ ଉତ୍ସ ହେଉଛି ଭୂତ୍ଵକ୍ (Earth’s crust)
- ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ ଓ ମ୍ୟାଗ୍ନେସିୟମ କ୍ଲୋରାଇଡ୍ ଇତ୍ୟାଦି ଦ୍ରବଣୀୟ ଲବଣ ସମୁଦ୍ର ଜଳରେ ମିଶିଥା’ନ୍ତି ।
- ପ୍ରକୃତିରେ ଭୂତ୍ଵକ୍ରୁ ମିଳୁଥିବା ମୌଳିକ ବା ଯୌଗିକକୁ ଖଣିଜ କୁହାଯାଏ ।
- କେତେକ ସ୍ଥାନରେ ଖଣିଜର ଅଧ୍ଵ ପ୍ରତିଶତମାତ୍ରାର ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ଧାତୁ ରହିଥାଏ ଏବଂ ସେହି ଖଣିଜରୁ ଧାତୁକୁ ନିଷ୍କାସନ କରିବା ଲାଭଜନକ ହୋଇଥାଏ । ଏହିସବୁ ଖଣିଜକୁ ଓର୍ ବା ଧାତୁପିଣ୍ଡ କୁହାଯାଏ ।
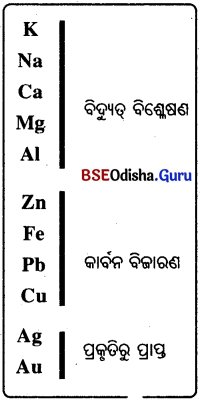
→ ଧାତୁ ନିଷ୍କାନ (Extraction of Metals) :
କିଛି ଧାତୁ ମୁକ୍ତ ଅବସ୍ଥାରେ ପୃଥିବୀର ଭୂତ୍ଵକ୍ରେ ମିଳିଥାନ୍ତି । ଉଦାହରଣସ୍ୱରୂପ, ସୁନା, ପ୍ଲାଟିନମ୍, ରୁପା, ତମ୍ବା ।
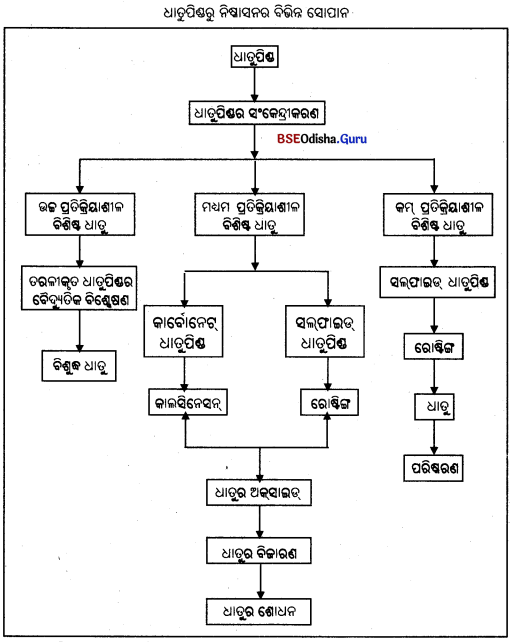
- ସକ୍ରିୟତା ଅନୁକ୍ରମର ନିମ୍ନଭାଗରେ ଥିବା ଧାତୁଗୁଡ଼ିକ କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ । ସେମାନେ ମୁକ୍ତ ଅବସ୍ଥାରେ କ୍ବଚିତ୍
- ତମ୍ବା ଏବଂ ରୁପା ସଲଫାଇଡ୍ ବା ଅକ୍ସାଇଡ୍ ଧାତୁପିଣ୍ଡ ଆକାରରେ ମଧ୍ୟ ଦେଖିବାକୁ ମିଳେ ।
- ସକ୍ରିୟତା ଅନୁକ୍ରମର ଊର୍ଦ୍ଧ୍ବରେ ଥିବା ଧାତୁଗୁଡ଼ିକ (K, Na, Ca, Mg, Al) ଏତେ ପ୍ରତିକ୍ରିୟାଶୀଳ ଯେ, ତାହା ପ୍ରକୃତିରେ ମୁକ୍ତ ମୌଳିକ ଅବସ୍ଥାରେ ମିଳେ ନାହିଁ ।
- ସକ୍ରିୟତା ଅନୁକ୍ରମର ମଝିରେ ଥିବା Zn, Pb, Fe ଇତ୍ୟାଦି ଧାତୁଗୁଡ଼ିକ ମଧ୍ୟମ ଧରଣର ପ୍ରତିକ୍ରିୟାଶୀଳ । ସେଗୁଡ଼ିକ ଭୂତ୍ଵକ୍ରେ ଅକ୍ସାଇଡ୍, ସଲଫାଇଡ୍ କିମ୍ବା କାର୍ବୋନେଟ୍ ରୂପରେ ମିଳିଥାଏ ।
- ଅଧିକାଂଶ ଧାତୁର ଧାତୁପିଣ୍ଡ ହେଉଛି ଅକ୍ସାଇଡ୍ । କାରଣ ଅକ୍ସିଜେନ୍ ଅତି ପ୍ରତିକ୍ରିୟାଶୀଳ ମୌଳିକ ଏବଂ

ବିଭକ୍ତ କରାଯାଇଛି ।- କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ବିଶିଷ୍ଟ ଧାତୁ
- ମଧ୍ୟମ ପ୍ରତିକ୍ରିୟାଶୀଳ ବିଶିଷ୍ଟ ଧାତୁ
- ଡଇ ପ୍ରତିକ୍ରିୟାଶୀଳ ବିଶିଷ୍ଟ ଧାତୁ
![]()
→ ଧାତୁପିଣ୍ଡରୁ ସମୃଦ୍ଧି (Enrichment of Ores) :
- ପୃଥିବୀର ଖଣିରୁ ବାହାରୁଥିବା ଧାତୁ ପିଣ୍ଡଗୁଡ଼ିକ ଅନେକ ପରିମାଣର ଅପଦ୍ରବ; ଯଥା – ମାଟି, ବାଲି ଇତ୍ୟାଦି ଦ୍ଵାରା ଦୂଷିତ ହୋଇଥାଏ । ତାହାକୁ ଗାଈ (Gangue) କୁହାଯାଏ ।
- ଗାଙ୍ଗ୍ ଓ ଧାତୁପିଣ୍ଡ ମଧ୍ୟରେ ଥିବା ଭୌତିକ ଓ ରାସାୟନିକ ଧର୍ମଗତ ପାର୍ଥକ୍ୟକୁ ନେଇ ଧାତୁପିଣ୍ଡରୁ ଗାଈକୁ ଅଲଗା କରାଯାଏ ।
(a) ସକ୍ରିୟତା କ୍ରମର ନିମ୍ନରେ ଥିବା ଧାତୁଗୁଡ଼ିକର ନିଷ୍କାସନ (Extracting Metals Low in the Activity Series) :
ସକ୍ରିୟତା କ୍ରମର ନିମ୍ନରେ ଥିବା ଧାତୁଗୁଡ଼ିକ ଅତ୍ୟନ୍ତ ଅଣପ୍ରତିକ୍ରିୟାଶୀଳ (unreactive) । ପୃଥକ୍ ଭାବେ ଉତ୍ତପ୍ତ କରି ଏହି ଧାତବ ଅକ୍ସାଇଡ୍ ଧାତୁରେ ପରିଣତ କରାଯାଏ ।
→ ଉଦାହରଣ :
- ମରକ୍ୟୁରି ଧାତୁପିଣ୍ଡର ନାମ ସିନାବାର (HgS) । ଏହାକୁ ବାୟୁରେ ଉତ୍ତପ୍ରକଲେ ମରକ୍ୟୁରିକ୍ ଅକ୍ସାଇଡ୍ (HgO) ରେ ପରିଣତ ହୁଏ । ଏହାକୁ ଆହୁରି ଉତ୍ତପ୍ତ କଲେ ମର୍କ୍ୟୁରିକ୍ ଅକ୍ସାଇଡ୍ ବିଜାରିତ ହୋଇ ମରକ୍ୟୁରି ମିଳେ ।
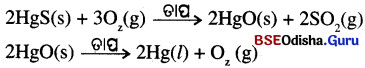
- ସେହିପରି Cu S ଧାତୁପିଣ୍ଡରୁ ତମ୍ବା ପାଇବାପାଇଁ ଏହାକୁ ବାୟୁରେ ଉତ୍ତପ୍ତ କରାଯାଏ ।
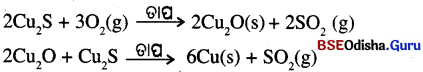
(b) ମଧ୍ୟମ କ୍ରମର ସକ୍ରିୟ ଧାତ୍ର ନିଷ୍କାସନ (Extracting Metals in the Middle of the Activity series)
ସକ୍ରିୟତା କ୍ରମର ମଧ୍ୟରେ ଥିବା ଧାତୁଗୁଡ଼ିକ; ଯଥା – ଲୁହା, ଜିଙ୍କ୍, ଲେଡ୍ , କପର ଇତ୍ୟାଦି ଧାତୁ ମଧ୍ୟମ ଧରଣର ପ୍ରତିକ୍ରିୟାଶୀଳ ।
ଏଗୁଡ଼ିକ ସାଧାରଣତଃ ସଲ୍ଫାଇଡ୍ କିମ୍ବା କାର୍ବୋନେଟ୍ ରୂପରେ ପ୍ରକୃତିରେ ମିଳିଥାଏ । ଏହାର ନିଷ୍କାସନ ପାଇଁ ତିନୋଟି ପଦ୍ଧତି ଅବଲମ୍ବନ କରାଯାଏ ।
- ରୋଷ୍ଟିଙ୍ଗ – ସଲ୍ଫାଇଡ୍ ଓରକୁ ଅକ୍ସାଇଡ୍ରେ ପରିଣତ କରିବାକୁ ହେଲେ ଏହାକୁ ଯଥେଷ୍ଟ ପରିମାଣର ବାୟୁର ଉପସ୍ଥିତିରେ ଅଧୂକ ପରିମାଣରେ ଉତ୍ତପ୍ତ କରାଯାଏ । ଏହି ପ୍ରଣାଳୀକୁ ରୋଷ୍ଟିଙ୍ଗ କହନ୍ତି ।
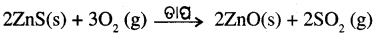
- କାଲସିନେସନ୍ – ସୀମିତ ପରିମାଣ ବାୟୁରେ କାର୍ବୋନେଟ୍ ଧାତୁପିଣ୍ଡକୁ ଉତ୍ତପ୍ତ କରି ଅକ୍ସାଇଡ୍ରେ ପରିଣତ କରାଯାଏ । ଏହି ପ୍ରଣାଳୀକୁ କାଲସିନେସନ୍ (Calcination) କହନ୍ତି ।
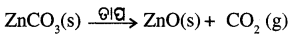
- ବିଜାରଣ – ଧାତବ ଅକ୍ସାଇଡ୍ କାର୍ବନ ପରି ଉପଯୁକ୍ତ ବିଜାରଣ ଦ୍ଵାରା ଉପଯୋଗୀ ଧାତୁକୁ ବିଜାରିତ ହୋଇଥାଏ । ଉଦାହରଣ ସ୍ଵରୂପ ଯେତେବେଳେ ଜିଙ୍କ୍ ଅକ୍ସାଇଡ୍କୁ କାର୍ବନ ସହିତ ଉତ୍ତପ୍ତ କରାଯାଏ, ତାହା ଧାତବ ଜିକୁ ବିଜାରିତ ହୁଏ ।
ZnO(s) + C(s) → Zn(s) + CO(g) - ଅଧିକ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁ; ଯଥା— ସୋଡ଼ିୟମ୍, କ୍ୟାଲସିୟମ୍, ଏଲୁମିନିୟମ୍ ଇତ୍ୟାଦି ମଧ୍ୟ ବିଜାରକ ରୂପେ କାମକଲେ କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁକୁ ସେମାନଙ୍କ ଯୌଗିକରୁ ଅପସାରଣ କରନ୍ତି ।
→ ଉଦାହରଣ :
- ଏଲୁମିନିୟମ୍ କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁ Mnକୁ ଯୌଗିକରୁ ଅପସାରଣ କରେ ।
- ଏହି ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାଟି ଅତିମାତ୍ରାରେ ତାପ ଉତ୍ପାଦୀ ଅଟେ, ଉତ୍ପନ୍ନ ହେଉଥିବା ତାପର ପରିମାଣ ଏତେ ଅଧୂକ ଯେ, ଧାତୁଗୁଡ଼ିକ ତରଳ ଅବସ୍ଥାରେ ସୃଷ୍ଟି ହୁଅନ୍ତି ।
3MnO2(s) + 4Al(s) → 3Mn (l) + 2Al2O3(s)
→ ଥରମିଟ (Thermit) ପ୍ରତିକ୍ରିୟା:
- ଫେରିକ୍ ଅକ୍ସାଇଡ୍ (Fe2O3) ର ଏଲୁମିନିୟମ୍ ସହ ପ୍ରତିକ୍ରିୟା ରେଳଧାରଣାଗୁଡ଼ିକୁ ଯୋଡ଼ିବାରେ କିମ୍ବା ଫାଟିଯାଇଥବା ଯନ୍ତ୍ରାଂଶକୁ ଯୋଡ଼ିବା ପାଇଁ ବ୍ୟବହୃତ ହୁଏ । ଏପରି ଯୋଡ଼ିବା ପ୍ରତିକ୍ରିୟାକୁ ଥରମିଟ୍ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ ।
Fe2O3(s) + 2Al(s) ) → 2Fe(l) + Al2O3(s) + ଚାପ
![]()
(c) ଅଧ୍ଵ ସକ୍ରିୟତା କ୍ରମର ଧାତବ ନିଷ୍କାସନ (Extracting Metals towards the top of the Activity series):
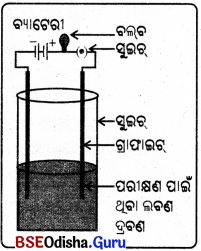
ପ୍ରତିକ୍ରିୟାଶୀଳତା କ୍ରମର ଊର୍ଦ୍ଧ୍ବରେ ଥିବା ଧାତୁଗୁଡ଼ିକ ଅଧିକ ପ୍ରତିକ୍ରିୟାଶୀଳ ଅଟେ । କାର୍ବନ ସହ ଉତ୍ତପ୍ତ କରି ସେଗୁଡ଼ିକୁ ସେମାନଙ୍କ ଯୌଗିକରୁ ପାଇପାରିବା ନାହିଁ । କାରଣ ଏହି ଧାତୁଗୁଡ଼ିକ ବୈଦ୍ୟୁତିକ ବିଜାରଣ ଦ୍ଵାରା ମିଳିଥାଏ ।
→ ଉଦାହରଣ :
- ସୋଡ଼ିୟମ୍, ମ୍ୟାଗ୍ନେସିୟମ୍ ଏବଂ କ୍ୟାଲସିୟମ୍ ତରଳ କ୍ଲୋରାଇଡ୍କୁ ବୈଦ୍ୟୁତିକ ବିଶ୍ଳେଷଣ ଦ୍ବାରା ମିଳିଥାଏ ।
- ଧାତୁଗୁଡ଼ିକ କ୍ୟାଥୋଡ଼ଠାରେ ଜମାହେଲାବେଳେ କ୍ଲୋରିନ୍ ଏନୋଡ୍ଠାରେ ନିର୍ଗତ ହୁଏ ।
କ୍ୟାଥୋଡ଼ଠାରେ Na+ + e– → Na
ଏନୋଡ୍ଠାରେ 2Cl– → Cl2 + 2e–
→ ଧାତ୍ରୀର ପରିଷ୍କରଣ (Refining of Metals):
- ବିଭିନ୍ନ ବିଜାରଣ ପ୍ରଣାଳୀରେ ଉତ୍ପନ୍ନ ହେଉଥିବା ଧାତୁଗୁଡ଼ିକ ମମ୍ପୂର୍ଣଭାବେ ବିଶୁଦ୍ଧ ନୁହଁନ୍ତି । ଅଶୁଦ୍ଧ ଧାତୁକୁ ଶୁଦ୍ଧ କରିବା ପାଇଁ ବୈଦ୍ୟୁତିକ ପରିଷ୍କରଣ ପ୍ରଣାଳୀ ଅବଲମ୍ବନ କରାଯାଏ।
- ବୈଦ୍ୟୁତିକ ବିଶୋଧନ – କପର୍, ଜିଙ୍କ, ଟିନ୍, ନିକେଲ୍, ରୁପା, ସୁନା ଇତ୍ୟାଦିକୁ ବୈଦ୍ୟୁତିକ ବିଶୋଧନ କରାଯାଏ ।
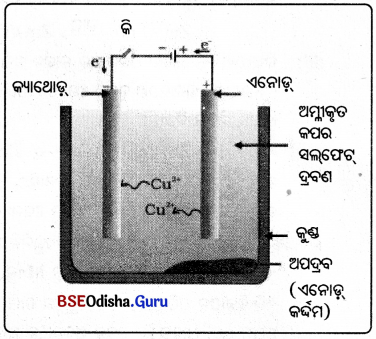
- ଏହି ପ୍ରଣାଳୀରେ ଅଶୋଧୃ ଧାତୁକୁ ଏନୋଡ଼ ଏବଂ ଏକ ବିଶୁଦ୍ଧ ଧାତୁର ପତଳା ପାତକୁ କ୍ୟାଥୋଡ଼ ରୂପେ ନିଆଯାଏ ।
- ସେହି ଧାତୁର କୌଣସି ଏକ ଲବଣର ଦ୍ରବଣକୁ ବିଦ୍ୟୁତ୍ ବିଶ୍ଳେଷ୍ୟ ରୂପେ ନିଆଯାଏ ।
- ବିଦ୍ୟୁତ୍ ବିଶ୍ଳେଷ୍ୟରେ ବିଦ୍ୟୁତ୍ ସ୍ରୋତ ପ୍ରବାହ କରିବା ଦ୍ଵାରା ଏନୋଡ଼ର ବିଶୁଦ୍ଧ ଧାତୁ ବିଦ୍ୟୁତ୍ ବିଶ୍ଳେଷ୍ୟରେ ଦ୍ରବୀଭୂତ ହୋଇ ଯାହା ସମ ପରିମାଣରେ ବିଶୁଦ୍ଧ ଧାତୁ କ୍ୟାଥୋଡ୍ ଉପରେ ଜମାହୁଏ ।
- ଦ୍ରବଣୀୟ ଅପଦ୍ରବ ଦ୍ରବଣରେ ମିଶିଥାଏ ଓ ଅଦ୍ରବଣୀୟ ଅପଦ୍ରବ ଏନୋଡ୍ର ବସିଥାଏ । ଏହାକୁ ଏନୋଡ୍ କର୍ଦ୍ଦମ କରନ୍ତି
→ ସଂକ୍ଷାରଣ (Corrosion):
- କେତେକ ଧାତୁ ଆର୍ଦ୍ରବାୟୁ ସଂସ୍ପର୍ଶରେ ମୁକ୍ତ ଅବସ୍ଥାରେ ରହିଲେ ବାୟୁ, ଜଳ ଓ ଅନ୍ୟ କେତେକ ଦ୍ରବ୍ୟ ସହିତ ପ୍ରତିକ୍ରିୟାକରି ଏକ ଆବରଣ ସୃଷ୍ଟି ହୁଏ ।
- ଏହି ପ୍ରକ୍ରିୟାକୁ ସଂକ୍ଷାରଣ କହନ୍ତି ।
→ ଉଦାହରଣ :
- ରୁପା ବାୟୁରେ ରହିଲେ ବାୟୁରେ ଥିବା ସଲଫର ରୁପା ସହିତ ପ୍ରତିକ୍ରିୟାକରି ସିଲଭର ସଲ୍ଫାଇଡ୍ର ଏକ କଳା ରଙ୍ଗର ଆବରଣ ଏହା ଉପରେ ସୃଷ୍ଟିକରେ ।
- କପର ବାୟୁରେ ଥିବା ଆର୍ଦ୍ର ଅଙ୍ଗାରକାମ୍ଳ ସହ ପ୍ରତିକ୍ରିୟା କରି କପର କାର୍ବୋନେଟ୍ର ଏକ ସବୁଜ ଆବରଣ ସୃଷ୍ଟି କରେ ।
- ଲୁହା ଆର୍ଦ୍ର ବାୟୁରେ ବହୁତ ସମୟ ରହିଲେ ଏଥିରେ ବାଦାମୀ ପତଳା ଆଚ୍ଛାଦନ ଲାଭ କରିଥାଏ । ଏହାକୁ
ଲୁହାରେ କଳଙ୍କି ଧରେ:
