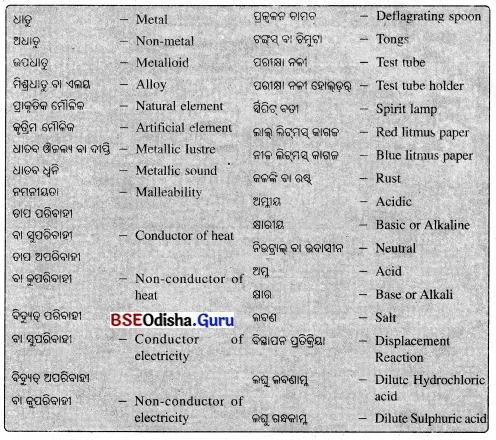
Odisha State Board BSE Odisha 8th Class Science Notes Chapter 4 ଧାତୁ ଓ ଅଧାତୁ will enable students to study smartly.
BSE Odisha Class 8 Science Notes Chapter 4 ଧାତୁ ଓ ଅଧାତୁ
→ ଉପକ୍ରମ : (Introduction):
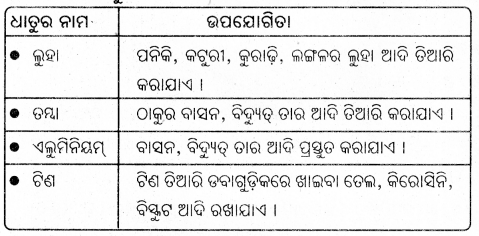
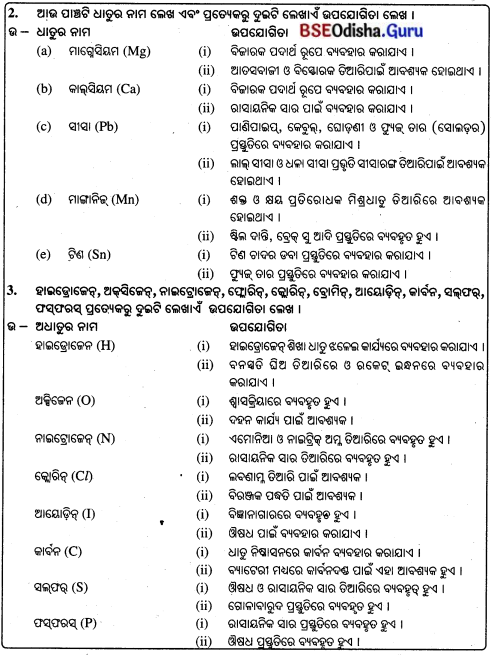
କେତେକ ଧାତୁର ନାମ ଓ ଏହାର ଉପଯୋଗିତା
![]()
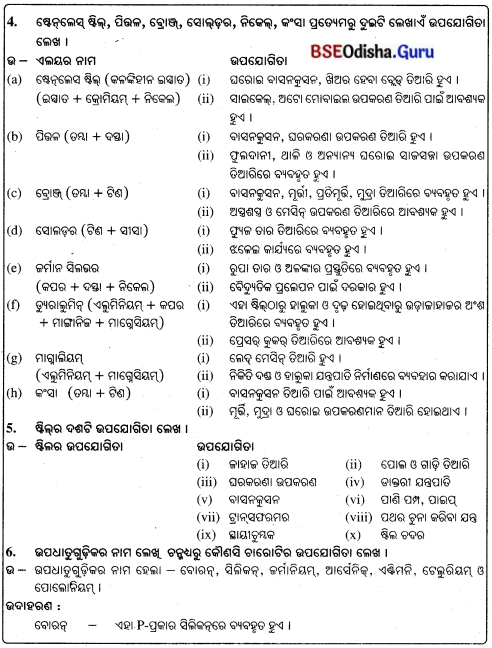
କେତେକ ଅଧାତୁର ନାମ ଓ ଏହାର ଉପଯୋଗିତା

(i) ଆଧୁନିକ ବିଜ୍ଞାନରେ ମୌଳିକଗୁଡ଼ିକୁ ମୁଖ୍ୟତଃ ଧାତୁ ଓ ଅଧାତୁ ଶ୍ରେଣୀଭୁକ୍ତ କରାଯାଇଛି । ଏହା ବ୍ୟତୀତ କେତେକ ମୌଳିକ ମଧ୍ୟ ଉପଧାତୁ ଶ୍ରେଣୀର ଅଟନ୍ତି ।
(ii) ଯେଉଁ ମୌଳିକଗୁଡ଼ିକର ଧାତବ ପ୍ରକୃତି ଅଧିକ ମାତ୍ରାରେ ଦେଖାଯାଏ, ସେଗୁଡ଼ିକୁ ଧାତୁ (Metal) କୁହାଯାଏ । ଲୁହା, ତମ୍ବା, ଏଲୁମିନିୟମ୍, ଟିଣ ଆଦି ଧାତୁ ଅଟନ୍ତି ।
(iii) ଯେଉଁ ମୌଳିକଗୁଡ଼ିକର ଧାତବ ପ୍ରକୃତି ଅତି କମ୍ ମାତ୍ରାରେ ଦେଖାଯାଏ, ସେଗୁଡ଼ିକୁ ଅଧାତୁ (Non-metal) କୁହାଯାଏ । କାର୍ବନ, ସଲ୍ଫର୍, ଫସ୍ଫରସ୍, ଆୟୋଡ଼ିନ୍ ଆଦି ଅଧାତୁ ଅଟନ୍ତି ।
(iv) ଯେଉଁ ମୌଳିକଗୁଡ଼ିକ ଉଭୟ ଧାତୁ ଓ ଅଧାତୁର ଧର୍ମ ପ୍ରଦର୍ଶନ କରିଥା’ନ୍ତି ସେଗୁଡ଼ିକୁ ଉପଧାତୁ (Metalloid) କୁହାଯାଏ । ବୋରନ୍, ସିଲିକନ୍, ଜର୍ମାନିୟମ୍, ଆର୍ସେନିକ୍, ଏଣ୍ଟ୍ରିମନି ଆଦି ଉପଧାତୁ ଅଟନ୍ତି ।
(v) ଏବଂ ଅଧିକ ସଂଖ୍ୟକ ଅଶ୍ମମଣ୍ଡଳରେ ଦେଖାଯାଆନ୍ତି । ଏଗୁଡ଼ିକ ସବୁ ପ୍ରକୃତିରେ ଉପଲବ୍ଧ ହେଉଥିବାରୁ ଏଗୁଡ଼ିକୁ ପ୍ରାକୃତିକ ମୌଳିକ (Natural Elemenis) କୁହାଯାଏ ।
1. ଗୋଟିଏ ତରଳ ଧାତୁ ଓ ଗୋଟିଏ ତରଳ ଅଧାତୁର ନାମ ଲେଖ ।
ଊ-
ତରଳ ଧାତୁ – ପାରଦ, ତରଳ ଅଧାତୁ – କ୍ରୋମିନ୍
2. ଗ୍ୟାସୀୟ ଅଧାତୁଗୁଡ଼ିକର ନାମ ଲେଖ ।
ଉ-
ହାଇଡ୍ରୋଜେନ୍, ନାଇଟ୍ରୋଜେନ୍, ଅକ୍ସିଜେନ୍, ଫ୍ଲୋରିନ୍, କ୍ଲୋରିନ୍, ହିଲିୟମ୍, ନିୟନ୍, ଆରଗନ୍, କ୍ରିପଟନ୍, ଜେନନ୍ ଓ ରେଡ଼ନ୍ ଆଦି ଗ୍ୟାସୀୟ ଅଧାତୁ ଅଟନ୍ତି ।
3. ଗ୍ୟାସୀୟ ଧାତୁ ସମ୍ବନ୍ଧରେ ତଥ୍ୟ ସଂଗ୍ରହ କର ।
ଉ-
କୌଣସି ଧାତୁ ଗ୍ୟାସୀୟ ଅବସ୍ଥାରେ ନଥାନ୍ତି ।
4. କୃତ୍ରିମ ମୌଳିକ ସମ୍ବନ୍ଧରେ ତଥ୍ୟ ସଂଗ୍ରହ କର ।5.
ଉ-
ବିଜ୍ଞାନାଗାରରେ ପ୍ରସ୍ତୁତ ହୋଇଥିବା ମୌଳିକଗୁଡ଼ିକୁ କୃତ୍ରିମ ମୌଳିକ କୁହାଯାଏ । ବର୍ତମାନ ସୁଦ୍ଧା ଏଗୁଡ଼ିକର ସଂଖ୍ୟା 20 ରୁ 25 ମଧ୍ୟରେ ସୀମିତ I କୃତ୍ରିମ ମୌଳିକ ପ୍ରସ୍ତୁତି କାର୍ଯ୍ୟକ୍ରମ ପୃଥିବୀର ବିଭିନ୍ନ ରାଷ୍ଟ୍ରରେ କାର୍ଯ୍ୟକାରୀ ହେଉଛି ।
5. ମିଶ୍ରଧାତୁ ବା ଏଲୟ କ’ଣ ତଥ୍ୟ ସଂଗ୍ରହ କର ।
ଉ-
(i) ଧାତୁ ଓ ଅଧାତୁ କିମ୍ବା ଧାତୁ ଓ ଧାତୁ କିମ୍ବା ଧାତୁ ଓ ଉପଧାତୁର ମିଶ୍ରଣକୁ ମିଶ୍ରଧାତୁ ବା ଏଲୟ କୁହାଯାଏ ।
(ii) ଉଚ୍ଚ ତାପମାତ୍ରାରେ ଉତ୍ତପ୍ତ କରି ଏଗୁଡ଼ିକୁ ତରଳାବସ୍ଥାକୁ ଅଣାଯାଏ ଓ ତା’ପରେ ଆବଶ୍ୟକ ଅନୁପାତରେ ସେଗୁଡ଼ିକୁ ମିଶାଯାଏ । ଶୀତଳ ହୋଇ ମିଶ୍ରଣଟି କଠିନାବସ୍ଥାକୁ ଆସେ । ଏହି କଠିନ ପଦାର୍ଥକୁ ଏଲୟ କୁହାଯାଏ ।
(iii) ଦୁଇ କିମ୍ବା ଦୁଇରୁ ଅଧିକ ମୌଳିକକୁ ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ଅନୁପାତରେ ନେଇ ବିଭିନ୍ନ ପ୍ରକାର ଏଲୟ ପ୍ରସ୍ତୁତ କରାଯାଏ । ଉଦାହରଣ : ଲୁହା + କାର୍ବନ = ଇସ୍ପାତ; ତମ୍ବା + ଦସ୍ତା = ପିତ୍ତଳ ।
ପଦାର୍ଥର ଧର୍ମଗୁଡ଼ିକୁ ଦୁଇଟି ବିଭାଗରେ ବିଭକ୍ତ କରାଯାଏ; ଯଥା – ଭୌତିକ ଧର୍ମ (Physical Properties), ରାସାୟନିକ ଗୁଣ (Chemical Properties) ।
→ ଧାତୁର ଶାରୀରିକ ଗୁଣ (Physical Properties of Metals) :
(i) ଅଧିକାଂଶ ଧାତୁ ନୂତନ ଅବସ୍ଥାରେ ଅର୍ଥାତ୍ ପ୍ରସ୍ତୁତିବେଳେ ଚକ୍ରଚକ୍ ଦେଖାଯା’ନ୍ତି; କିନ୍ତୁ ପୁରୁଣା ହୋଇଗଲେ ଫିକା ବା ମଳିନ ଦେଖାଯା’ନ୍ତି । ଧାତୁର ଚକ୍କ୍ ରୂପ ବା ଧର୍ମକୁ ଧାତବ ଦୀପ୍ତି ବା ଔଜଲ୍ୟ (Metallic lustre) କୁହାଯାଏ ।
ପ୍ର. ବାଲିକାଗଜ ଘସିବା ପୂର୍ବରୁ ଧାତୁଗୁଡ଼ିକ କାହିଁକି ମଳିନ ଦେଖାଯାଉଥିଲା ଓ ବାଲି କାଗଜ ଘଷିଲା ପରେ ତାହା ଚକ୍ଚକ୍ ଦେଖାଗଲା, କାରଣ କ’ଣ ?
ଉ-
ଗୋଟିଏ ଧାତବ ବସ୍ତୁ କିଛିଦିନ ରହିଗଲେ ବାୟୁର ଅମ୍ଳଜାନ ସଂସ୍ପର୍ଶରେ ଆସି ସେଥୁରେ ଅକ୍ସାଇଡ୍ ଯୌଗିକ ସୃଷ୍ଟି ହୁଏ; ଫଳରେ ତାହା ମଳିନ ଦେଖାଯାଏ । ବାଲିକାଗଜରେ ଘଷିବା ପରେ ଅକ୍ସାଇଡ୍ ଯୌଗିକ ପରିଷ୍କାର ହୋଇଯିବାରୁ ତାହା ପୁନର୍ବାର ଚକ୍ ଚକ୍ ଦେଖାଯାଏ ।
(ii) ଅଧିକାଂଶ ଧାତୁ ପ୍ରସାରଣଶୀଳ ବା ନମନୀୟ (Malleability) । ଏହି ଗୁଣ ଯୋଗୁଁ ବିଭିନ୍ନ ଧାତୁର ଚଦର
(iii) ଧାତୁ ତାପ ପରିବହନ କରେ, ଅର୍ଥାତ୍ ଧାତୁଗୁଡ଼ିକ ତାପ ପରିବାହୀ (Conductors of heat) ।
(iv) ଧାତୁ ବିଦ୍ୟୁତ୍ ପରିବହନ କରେ; ଅର୍ଥାତ୍ ଧାତୁଗୁଡ଼ିକ ବିଦ୍ୟୁତ୍ ପରିବାହୀ (Conductors of electricity) ଅଟନ୍ତ ।
(v) ଲୁହା, ତମ୍ବା, ଏଲୁମିନିୟମ୍, ସୁନା, ରୁପା ଆଦି ଧାତୁକୁ ତରଳାଇ ସ୍ୱତନ୍ତ୍ର ଯନ୍ତ୍ରଦ୍ବାରା ଭିନ୍ନ ଭିନ୍ନ ମୋଟେଇର ତାର ପ୍ରସ୍ତୁତ କରାଯାଇଛି । ଧାତୁଗୁଡ଼ିକର ତାରରେ ରୂପାନ୍ତରଣ ହେବା ଗୁଣ ବା ପ୍ରକୃତିକୁ ତନ୍ୟତା (Ductility) ଧର୍ମ କୁହାଯାଏ ।
(vi) ଧାତୁଗୁଡ଼ିକରୁ ସୃଷ୍ଟି ହେଉଥିବା ଧ୍ଵନି ବା ଶବ୍ଦକୁ ଧାତବ ଧ୍ବନି କୁହାଯାଏ । ସାଧାରଣତଃ ଅଧିକାଂଶ ଧାତୁରୁ ଏଭଳି ଶବ୍ଦ ବା ଧ୍ୱନି ସୃଷ୍ଟି ହେଉଥିବାରୁ ଏହାକୁ ଧାତୁଗୁଡ଼ିକର ଏକ ଧର୍ମ ରୂପେ ବିବେଚନା କରାଯାଏ ।
(vii) ଅଧିକାଂଶ ଧାତୁ ଶକ୍ତ ବା ଟାଣ ଅଟେ !
![]()
ପାରଦ ( ଧାତୁ) ସାଧାରଣ ତାପମାତ୍ରାରେ ତରଳ ଅବସ୍ଥାରେ ଥାଏ ।
କେତେକ ଧାତୁଗୁଡ଼ିକ ଧର୍ମରେ ବ୍ୟତିକ୍ରମ –
ସୋଡ଼ିୟମ୍ ଓ ପୋଟାସିୟମ୍ ପରି ଧାତୁ ନରମ ଅଟନ୍ତି ଏବଂ ଛୁରୀ ସାହାଯ୍ୟରେ କାଟି ହୁଏ । ପାରଦ ଏକମାତ୍ର ଧାତୁ-
ଯାହା ସାଧାରଣ ତାପମାତ୍ରାରେ ତରଳ ଅବସ୍ଥାରେ ରହିଥାଏ ।
ପ୍ରତ୍ୟେକ ପରୀକ୍ଷଣ ନିମିତ୍ତ ନିମ୍ନ ସୋପାନଗୁଡ଼ିକୁ ଅନୁସରଣ କରାଯାଇଥାଏ ।
(i) ଆବଶ୍ୟକୀୟ ଉପକରଣର ଆବଶ୍ୟକତା (Apparatus required)
(i) ଆବଶ୍ୟକୀୟ ରାସାୟନିକ ପଦାର୍ଥ (Chemicals required)
(iii) ସଜ୍ଜିକରଣ ଏବଂ ପରୀକ୍ଷଣ ପ୍ରସ୍ତୁତି (Procedure)
(iv) ସୂଚନା (Inference)
ଉକ୍ତ କ୍ରମିକ ସୋପାନ ଭିତ୍ତିକ ପଦ୍ଧତିକୁ ‘ବୈଜ୍ଞାନିକ ପଦ୍ଧତି’ (Scientific Method) କୁହାଯାଏ !
ଅଣ ଧାତୁର ଶାରୀରିକ ଗୁଣ (Physical Properties of Non-metals):
(i) ଅଧାତୁଗୁଡ଼ିକ ଚକ୍ ଚକ୍ ଦେଖାଯା’ନ୍ତି ନାହିଁ (Non-lustrous) । ବ୍ୟତିକ୍ରମ – ଗ୍ରାଫାଇଟ୍, ଆୟୋଡ଼ିନ୍ ।
(ii) ଅଧାତୁଗୁଡ଼ିକ ନମନୀୟ ନୁହଁନ୍ତି (Non-malleable) । ଏଗୁଡ଼ିକ ଭଙ୍ଗୁର (Brittle) ।
(iii) ଅଧାତୁଗୁଡ଼ିକ ତାପ ଓ ବିଦ୍ୟୁତର କୁପରିବାହୀ ଅଟନ୍ତି । ବ୍ୟତିକ୍ରମ – ଗ୍ରା ଫାଇଟ୍
(iv) ଅଧାତୁଗୁଡ଼ିକ ତଥ୍ୟ ନୁହଁନ୍ତି (Non-ductile) ।
(v) ଅଧାତୁଗୁଡ଼ିକରୁ ଧ୍ୱନି ସୃଷ୍ଟି ହୁଏ ନାହିଁ (Non-sonorous) i
(vi) ଅଧାତୁଗୁଡ଼ିକ ନରମ (Soft) । ବ୍ୟତିକ୍ରମ – ହୀରା ।
(vi) ସାଧାରଣ ତାପମାତ୍ରାରେ ଏଗୁଡ଼ିକ କଠିନ କିମ୍ବା ଗ୍ୟାସୀୟ । ବ୍ୟତିକ୍ରମ – ବ୍ରୋମିନ୍ (ତରଳ) ।
(viii) ଏଗୁଡ଼ିକର ଗଳନାଙ୍କ ଓ ସ୍ଫୁଟନାଙ୍କ କମ୍ । ବ୍ୟତିକ୍ରମ – ଗ୍ରାଫାଇଟ୍ ।
(ix) ଏଗୁଡ଼ିକର ସାନ୍ଦ୍ରତା କମ୍ (Low density) ।
1. କାର୍ବନ – କୋଇଲାର ମୁଖ୍ୟ ଉପାଦାନ କାର୍ବନ୍ ହୋଇଥିବାରୁ କୋଇଲାକୁ କାର୍ବନର ନମୁନା ରୂପେ ନିଆଯାଇପାରେ । କୋଇଲା ନ ମିଳିଲେ କାଠ ଅଙ୍ଗାରକୁ ନମୂନା ରୂପେ ନିଆଯାଇପାରେ ।
2. ସଲ୍ଫର୍ – ଏହା ସାଧାରଣତଃ ହଳଦିଆ ଚୂର୍ଣ୍ଣ ରୂପେ ଉପଲବ୍ଧି ହୋଇଥାଏ । ଏହାକୁ କାଚ କିମ୍ବା ପ୍ଲାଷ୍ଟିକ୍ ବୋତଲରେ ରଖାଯାଇଥାଏ ।
3. ଫସ୍ଫରସ୍ – ଏହା ଏକ ନରମ ପଦାର୍ଥ ହୋଇଥିବାରୁ ଛୁରୀରେ କାଟି ଛୋଟ ଛୋଟ ଖଣ୍ଡ ବାହାର କରାଯାଏ । ଚଉଡ଼ା ମୁହଁଥିବା କାଚ ବୋତଲରେ ପରିଷ୍କାର ଜଳ ଭର୍ତ୍ତିକରି ସେଥିରେ ଫସ୍ଫରସ୍ ବଡ଼ ବଡ଼ ଖଣ୍ଡଗୁଡ଼ିକୁ ବୁଡ଼ାଇ ରଖାଯାଏ ।
4. ଆୟୋଡ଼ିନ୍ – ବାଇଗଣୀ ରଙ୍ଗର ଛୋଟ ଛୋଟ ଖଣ୍ଡ ରୂପେ ଏହା ମିଳେ । କାଠ ବୋତଲରେ ଏହା ରଖାଯାଏ ।
ଧାତୁ ଓ ଅଧାତୁଗୁଡ଼ିକର ରାସାୟନିକ ଧର୍ମ (Chemical Properties of Metals and Non-metals) :
ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ପଦାର୍ଥର ରାସାୟନିକ ଧର୍ମ କହିଲେ ଭିନ୍ନ ଭିନ୍ନ ପଦାର୍ଥ ସହ ସେହି ପଦାର୍ଥଟିର ପ୍ରତିକ୍ରିୟାକୁ ବୁଝାଏ । ଅକ୍ସିଜେନ, ଜଳ, ଅମ୍ଳ, କ୍ଷାର ଓ ଲବଣ ମଧ୍ୟରୁ ପ୍ରତ୍ୟେକ ସହ ଧାତୁର ପ୍ରତିକ୍ରିୟା ଏବଂ ପ୍ରତ୍ୟେକ ସହ ଅଧାତୁର ପ୍ରତିକ୍ରିୟା କିପରି
(a) ଧାତୁର ଅକ୍ସିଜେନ୍ ସହ ପ୍ରତିକ୍ରିୟା –
(i) ଲୁହା ଏବଂ ବାୟୁର ଅକ୍ସିଜେନ୍ ଓ ଜଳ ମଧ୍ୟରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସଂଘଟିତ ହୋଇ ଆଇରନ୍ ଅକ୍ସାଇଡ୍ ସୃଷ୍ଟି ହୁଏ; ଯାହାକୁ ରଷ୍ଟ୍ (Rust) ବା କଳଙ୍କି କୁହାଯାଏ ।
Fe + O2 + H2O → Fe2O3 (କଳଙ୍କି)
ଆଇରନ୍ + ଅକ୍ସିଜେନ୍ + ଜଳ → ଆଇରନ୍ ଅକ୍ସାଇଡ୍ ବା ଫେରିକ୍ ଅକ୍ସାଇଡ୍
1. ଧାତୁଗୁଡ଼ିକର ଭୌତିକ ଧର୍ମ ସହ ଅଧାତୁଗୁଡ଼ିକର ଭୌତିକ ଧର୍ମର ଏକ ତୁଳନାତ୍ମକ ବିବରଣୀ ଲେଖ ।
ଉ-
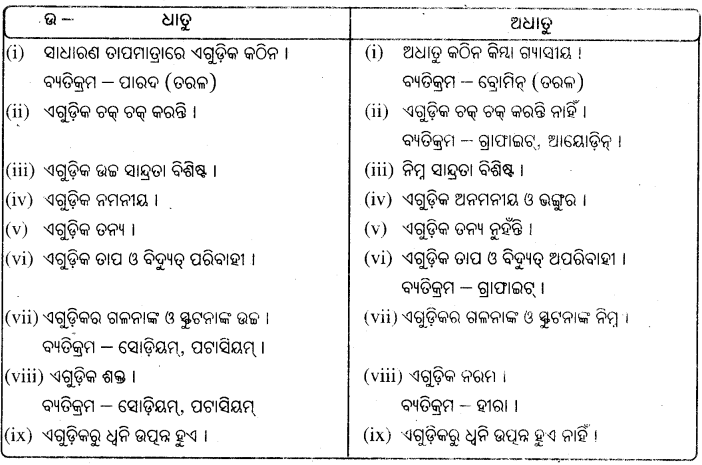
![]()
2. ଉଭୟଧର୍ମୀ ମୌଳିକଗୁଡ଼ିକ ମଧ୍ୟରୁ ଯେକୌଣସି ଦୁଇଟିର ନାମ ଲେଖ ।
ଉ-
(i) ବୋରନ୍
(ii) ସିଲିକନ୍
3. ଧାତବ ଔଜଲ୍ୟ ଓ ଧାତବ ଧ୍ଵନି ନଥିବା ଦୁଇଟି ଧାତୁର ନାମ ଲେଖ ।
ଊ –
(i) ଧାତବ ଔଜ୍ଜଲ୍ୟ ନ ଥିବା ଦୁଇଟି ଧାତୁ ହେଲା – ସୋଡ଼ିୟମ୍, ପଟାସିୟମ୍ ।
(ii) ଧାତବ ଧ୍ଵନି ନ ଥିବା ଦୁଇଟି ଧାତୁ ହେଲା – ପାରଦ, ସୁନା !
4. ତନ୍ୟତା ଓ ନମନୀୟତା ନଥିବା ଦୁଇଟି ଧାତୁର ନାମ ଲେଖ ।
ଉ-
(i) ପାରଦ,
(ii) ସୋଡ଼ିୟମ୍
5. ଔକ୍ସଲ୍ୟ ଥିବା ଗୋଟିଏ ଅଧାତୁର ନାମ ଲେଖ ।
ଉ-
ଗ୍ରାଫାଇଟ୍ ।
6. ଗୋଟିଏ ବିଦ୍ୟୁତ୍ ପରିବାହୀ ଅଧାତୁର ନାମ ଲେଖ ।
ଉ-
ଗ୍ରାଫାଇଟ୍ ।
7. ଲୁହାରେ ତିଆରି ଜିନିଷ ଉପରେ କଳଙ୍କି ନ ହେବା ପାଇଁ କି କି ପଦକ୍ଷେପ ନିଆଯାଏ ?
ଉ-
(i) ରଙ୍ଗ କିମ୍ବା ତେଲ ଲେପନ କରାଯାଏ ।
(ii) ଦସ୍ତା କିମ୍ବା ଟିଣ ଧାତୁର ଲେପନ କରାଯାଏ ।
8. ପୁରୁଣା କିମ୍ବା ଅବ୍ୟବହୃତ ତମ୍ବା ଓ ପିତ୍ତଳ ବାସନ ବା ସାମଗ୍ରୀ ଉପରେ ସବୁଜ ରଙ୍ଗର ଦାଗ କିପରି ହୋଇଥାଏ ?
ଉ-
ତମ୍ବା ଓ ପିତ୍ତଳ ସାମଗ୍ରୀ ଆର୍ଦ୍ର ବାୟୁ ସଂସ୍ପର୍ଶରେ ଦୀର୍ଘ ସମୟ ପାଇଁ ରହିଲେ ସବୁଜ ରଙ୍ଗର କପର କାର୍ବୋନେଟ୍ର ଆବରଣ ସୃଷ୍ଟି ହୁଏ ।
9. ତମ୍ବା + ଜଳ + ଅଙ୍ଗାରକାମ୍ଳ + ଅମ୍ଳଜାନ → କପର କାର୍ବୋନେଟ୍ + କପର ହାଇଡ୍ରକ୍ସାଇଡ଼
ଉ-
ଏଲୁମିନିୟମ୍ ଜିନିଷଗୁଡ଼ିକର ଦୀର୍ଘ ସମୟ ଧରି ବାୟୁ ସଂସ୍ପର୍ଶରେ ଆସିବା ଦ୍ଵାରା ସେଗୁଡ଼ିକର ଆବରଣରେ ଏଲୁମିନିୟମ୍ ଅକ୍ସାଇଡ୍ ସୃଷ୍ଟି ହୁଏ । ତେଣୁ ସେଗୁଡ଼ିକର ଔଜ୍ଜଲ୍ୟ ମଳିନ ଦେଖାଯାଏ ।
10. ଖଣ୍ଡିଏ ମାଗ୍ନେସିୟମ୍ ଫିତା ବାୟୁରେ ଜଳିଲେ କ’ଣ ହୁଏ ?
ଉ-
ଉ- ମାଗ୍ନେସିୟମ୍ ଫିତା ବାୟୁରେ ଜଳିଲେ ଉଜ୍ଜ୍ଵଳ ଆଲୋକ ପ୍ରଦାନ କରେ ଓ ଜଳିସାରିବା ପରେ ଧଳାରଙ୍ଗର ପାଉଁଶ ସୃଷ୍ଟି ହୁଏ । ସେହି ପାଉଁଶ ମ୍ୟାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ଼ ଅଟେ
ରଷ୍ଟ୍ ଓ ଜଳ ମଧ୍ୟରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସଂଘଟିତ ହୋଇ ଫେରିକ୍ ହାଇଡ୍ରିକ୍ସାଇଡ୍ ନାମକ ଏକ କ୍ଷାର ସୃଷ୍ଟି ହୁଏ, ଯାହାଦ୍ବାରା ଲାଲ ଲିଟ୍ମସ୍ ନୀଳ ହୁଏ । Fe22 + H2O → Fe(OH)3
ଆଇରନ୍ ଅକ୍ସାଇଡ୍ + ଜଳ → ଫେରିକ୍ ହାଇଡ୍ରିକ୍ସାଇଡ୍
1. ଯଦି କୌଣସି ଜଳୀୟ ମିଶ୍ରଣରେ ଲାଲ ଲିଟ୍ସ୍ କାଗଜ ବୁଡ଼ାଇଲେ ନୀଳ ହୋଇଯାଏ; ତେବେ ମିଶ୍ରଣ କ୍ଷାରୀୟ (Basic) ଅଟେ ।
(ମାଗ୍ନେସିୟମ୍ ଫିତାଟିଏ ବାୟୁରେ ଜଳିଲେ ମାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ୍ ଉତ୍ପନ୍ନ ହୁଏ ।
Mg + O2 → MgO (ମାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ୍)
MgO ଓ ଜଳ ମଧ୍ୟରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସଂଘଟିତ ହୋଇ ମାଗ୍ନେସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ ନାମକ ଏକ କ୍ଷାର ସୃଷ୍ଟି ହୁଏ, ଯାହାଦ୍ୱାରା ଲାଲ ଲିଟମସ୍ ନୀଳ ହୁଏ ।
MgO + H2O → Mg(OH), ମାଗ୍ନେସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ ସାଧାରଣତଃ ଧାତବ ଅକ୍ସାଇଡ୍ଗୁଡ଼ିକ କ୍ଷାରୀୟ ।
![]()
2. ଯଦି କୌଣସି ଜଳୀୟ ମିଶ୍ରଣରେ ନୀଳ ଲିଟ୍ମସ୍ ବୁଡ଼ାଇଲେ ଲାଲ ହୋଇଯାଏ; ତେବେ ମିଶ୍ରଣଟି ଅମ୍ଳୀୟ (Acidic) ଅଟେ ।
3. ଯଦି କୌଣସି ଜଳୀୟ ମିଶ୍ରଣରେ ଉଭୟ ଲିଟ୍ସ୍ କାଗଜର ରଙ୍ଗରେ କୌଣସି ପରିବର୍ତ୍ତନ ହୁଏ ନାହିଁ, ତେବେ ମିଶ୍ରଣଟି ନିଉଟ୍ରାଲ୍ (Neutral) ଅଟେ ।
→ ଅଧାତୁର ଅକ୍ସିଜେନ୍ ସହ ପ୍ରତିକ୍ରିୟା –
(i) ସଲଫର ବାୟୁରେ ଥିବା ଅକ୍ସିଜେନ୍କୁ ଉପଯୋଗ କରି ସଲ୍ଫର୍ ଡାଇଅକ୍ସାଇଡ୍ ଗ୍ୟାସ୍ ସୃଷ୍ଟି କରେ । ଏହି ଗ୍ୟାସ୍ ଜଳରେ ଦ୍ରବୀଭୂତ ହୋଇ ସଫ୍ୟୁରସ୍ ଅମ୍ଳ ସୃଷ୍ଟି କରେ । ଏହି ଅମ୍ଳ ଯୋଗୁଁ ନୀଳ ଲିଟ୍ସ୍ କାଗଜ ଲାଲ ହୁଏ ।
S+O2 → S + O2
SO2 + HO2 → H2SO3 (ସଲ୍ଫର୍ ଡାଇଅକ୍ସାଇଡ୍ + ଜଳ → ସଲ୍ଫ୍ୟୁରସ୍ ଅମ୍ଳ)
(ii) କୋଇଲା କିମ୍ବା ଅଙ୍ଗାର ଜାଳିଲେ ତାପଶକ୍ତି ସହ କାର୍ବନ ଡାଇଅକ୍ସାଇଡ୍ ଗ୍ୟାସ୍ (CO2) (ବର୍ଣ୍ଣହୀନ ଗ୍ୟାସ୍ ) ସୃଷ୍ଟି ହୁଏ । ଏହା ଜଳରେ କମ୍ ମାତ୍ରାରେ ଦ୍ରବଣୀୟ; କିନ୍ତୁ ଉଚ୍ଚ ତାପ ପ୍ରୟୋଗକଲେ ଅଧିକ ମାତ୍ରାରେ ଦ୍ରବଣୀୟ ହୋଇଥାଏ । ଏହି ଗ୍ୟାସ୍ ଜଳରେ ଦ୍ରବୀଭୂତ ହୋଇ କାର୍ବୋନିକ୍ ଅମ୍ଳ ସୃଷ୍ଟି କରେ ।
C + O2 → CO2
CO2 + HO2 → H2CO2. (କାର୍ବନ ଡାଇଅକ୍ସାଇଡ୍ + ଜଳ → କାର୍ବୋନିକ୍ ଅମ୍ଳ)
(iii) ଫସ୍ଫରସ୍ର ଛୋଟ ଖଣ୍ଡ ଚିନାମାଟି ପ୍ଲେଟ୍ରେ ଖୋଲାରେ ରଖିଲେ ବାୟୁର ଅକ୍ସିଜେନ୍ ସହ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କରି ଫସ୍ଫରସ୍ ପେଣ୍ଟାକ୍ସାଇଡ୍ ନାମକ ଧଳା ରଙ୍ଗର ଗ୍ୟାସ୍ ସୃଷ୍ଟି ହୁଏ, ଯାହାକି ଘନୀଭୂତ ହୋଇ ଧଳା ଚୂର୍ଣ୍ଣରେ ପରିଣତ ହୁଏ ।
P + O2 → P2O5 (ଫସ୍ଫରସ୍ ପେଣ୍ଟାକ୍ସାଇଡ୍)
P2O5 ଜଳରେ ଦ୍ରବୀଭୂତ ହୋଇ ତିନି ପ୍ରକାରର ଫସ୍ଫରିକ୍ ଅମ୍ଳ ସୃଷ୍ଟି କରେ ।
P2O5 + H2O → ଫସ୍ଫରିକ୍ ଅମ୍ଳ
ସାଧାରଣତଃ ଅଧାତୁଗୁଡ଼ିକର ଅକ୍ସାଇଗୁଡ଼ିକ ଅମ୍ଳୀୟ ଅଟନ୍ତି ।
(b) ଧାତୁର ଜଳ ସହ ପ୍ରତିକ୍ରିୟା –
ଧାତୁଗୁଡ଼ିକ ଜଳସହ ପ୍ରତିକ୍ରିୟା କରି ଧାତବ ହାଇଡ୍ରୋକ୍ସାଇଡ୍ ସୃଷ୍ଟି କରନ୍ତି ।
ଉଦାହରଣ :
(i) ସୋଡ଼ିୟମ୍ ଜଳ ସହ ତୀବ୍ର ପ୍ରତିକ୍ରିୟା କରି ସୋଡ଼ିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ ନାମକ କ୍ଷାର ସୃଷ୍ଟି କରିଥାଏ । ଏହା ଲାଲ୍ ଲିଟ୍ସ୍କୁ ନୀଳ କରିଥାଏ । ଏହାକୁ କିରୋସିନରେ ବୁଡ଼ାଇ ରଖାଯାଏ । Na+ H2O→→ NaOH
(ii) ପୋଟାସିୟମ୍ ମଧ୍ୟ ଜଳ ସହ ତୀବ୍ର ପ୍ରତିକ୍ରିୟା କରି ପୋଟାସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ (କ୍ଷାର) ଓ ତାପ ଶକ୍ତି ସୃଷ୍ଟି କରେ । ଏହା ଏକ କ୍ଷାର ଅଟେ ଏବଂ ଏହାକୁ ମଧ୍ୟ କିରୋସିନିରେ ବୁଡ଼ାଇ ରଖାଯାଏ । K + H2O → KOH
(iii) କାସିୟମ୍ ଓ ଲିଥ୍ୟମ୍ ଥଣ୍ଡା ଜଳ ସହ ପ୍ରତିକ୍ରିୟା କରି କ୍ଷାର ସୃଷ୍ଟି କରିଥା’ନ୍ତି । Ca + H2O → CaOH2
(iv) ମାଗ୍ନେସିୟମ୍ ଓ ଏଲୁମିନିୟମ୍ ଫୁଟନ୍ତା ଜଳ ସହ ପ୍ରତିକ୍ରିୟା କରି କ୍ଷାର ସୃଷ୍ଟି କରିଥା’ନ୍ତି । Mg + H2O → Mg(OH)2 ମାଗ୍ନେସିୟମ + ଜଳ → ମାଗ୍ନେସିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍
(v) ଲୁହାର ଜଳ ସହ ପ୍ରତିକ୍ରିୟା ବହୁତ ଧୀର ଗତିରେ ଘଟିଥାଏ ।
ସାଧାରଣତଃ ଜଳ ଓ ଅଧାତୁ ମଧ୍ୟରେ ପ୍ରତିକ୍ରିୟା ହୁଏ ନାହିଁ ।
(c) ଧାତୁର ଅମ୍ଳସହ ପ୍ରତିକ୍ରିୟା :
ଧାତୁଗୁଡ଼ିକ ଅମ୍ଳ ସହ ପ୍ରତିକ୍ରିୟା କରି ହାଇଡ୍ରୋଜେନ ଗ୍ୟାସ ଦହନ ହୁଏ ।
(i) କେତେକ ଧାତୁ ଓ ଲଘୁ ଲବଣାମ୍ଳ ମଧ୍ୟରେ ଏବଂ କେତେକ ଧାତୁ ଓ ଲଘୁ ଗନ୍ଧକାମ୍ଳ ମଧ୍ୟରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ସଂଘଟିତ ହୋଇ ହାଇଡ୍ରୋଜେନ୍ ଗ୍ୟାସ୍ ସୃଷ୍ଟି ହୁଏ । ଏହା ଏକ ଦହନୀୟ ଗ୍ୟାସ୍ ହୋଇଥିବାରୁ ଅଗ୍ନି ସଂସ୍ପର୍ଶରେ ଆସିବା କ୍ଷଣି ଦ୍ରୁତ ଦହନ ଯୋଗୁଁ ପପ୍ ଶବ୍ଦ ସୃଷ୍ଟି ହୁଏ ।
Na + HCI → NaC/ + H2 ↑
ସୋଡ଼ିୟମ୍ ସଲ୍ଫ୍ୟୁରିକ୍ ଏସିଡ୍ ସୋଡ଼ିୟମ୍ କ୍ଲୋରାଇଡ୍ ହାଇଡ୍ରୋଜେନ୍
(ii) କପର (ତମ୍ବା) ସହିତ ଲଘୁ ଲବଣାସ୍କର କୌଣସି ପ୍ରତିକ୍ରିୟା ହୁଏ ନାହିଁ । ଏପରିକି ଉତ୍ତପ୍ତ କଲେ ମଧ୍ୟ ନୁହେଁ । ତେଣୁ ଏ କ୍ଷେତ୍ରରେ ‘ପପ୍’ ଶବ୍ଦ ଶୁଭେ ନାହିଁ । ଅନ୍ୟ ପକ୍ଷରେ କପର୍ ଲଘୁ ଗନ୍ଧକାମ୍ଳ ସହ ପ୍ରତିକ୍ରିୟା କରିଥାଏ, ଫଳରେ ‘ପପ୍’ ଶବ୍ଦ ଶୁଭେ ।
Cu + H2SO4 → CuSO4 + H2
କପର ସଲ୍ଫେଟ୍ ହାଇଡ୍ରୋଜେନ
ଅଧାତୁଗୁଡ଼ିକ ଅମ୍ଳ ସହିତ ପ୍ରାୟତଃ ପ୍ରତିକ୍ରିୟା କରନ୍ତି ନାହିଁ ।
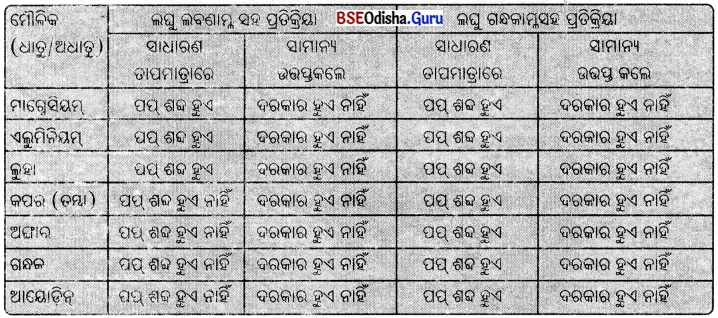
![]()
ବି.ଦ୍ର. : ଆୟୋଡ଼ିନ୍ ଓ ଅମ୍ଳଜାନ ମଧ୍ୟରେ କୌଣସି ପ୍ରତିକ୍ରିୟା ଘଟେ ନାହିଁ ।
(d) ଧାତୁର କ୍ଷାରସହ ପ୍ରତିକ୍ରିୟା –
(i) କେତେକ ଧାତୁ ଓ ସୋଡ଼ିୟମ୍ ହାଇଡ୍ରକ୍ସାଇଡ୍ (କ୍ଷାର) ମଧ୍ୟରେ ପ୍ରତିକ୍ରିୟା ସଂଘଟିତ ହୋଇ ହାଇଡ୍ରୋଜେନ୍ ସୃଷ୍ଟି ହୁଏ । ଉକ୍ତ ହାଇଡ୍ରୋଜେନ୍ର ଦହନ ଯୋଗୁଁ ‘ପପ୍’ ଶବ୍ଦ ସୃଷ୍ଟି ହୁଏ ।
(ii) ଆଲୁମିନିୟମ୍, ଜିଙ୍କ୍, ସୀସା କ୍ଷାରସହ ପ୍ରତିକ୍ରିୟା କରି ଧାତୁର ଲବଣ ଓ ଉଦ୍ଜାନ ଗ୍ୟାସ ସୃଷ୍ଟି କରନ୍ତି ।
(iii) ଅଧାତୁ ଓ କ୍ଷାର ମଧ୍ୟରେ ସଂଘଟିତ ପ୍ରତିକ୍ରିୟା ଅତି ଜଟିଳ ।
(e) ଧାତୁର ଲବଣ ସହ ପ୍ରତିକ୍ରିୟା।-
କେତେକ ଧାତୁ ଲବଣ ସହ ପ୍ରତିକ୍ରିୟା କରି ସେଥୁରୁ ଧାତୁକୁ ବିସ୍ଥାପିତ କରିଥାଏ । ଅଧିକ କ୍ରିୟାଶୀଳ ଧାତୁ କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁର ଲାବଣର ଦ୍ରବଣରୁ କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁକୁ ବିସ୍ଥାପିତ କରି ନିଜେ ସେହି ସ୍ଥାନ ଅଧିକାର କରେ । ଏହି ପ୍ରତିକ୍ରିୟାକୁ ବିସ୍ଥାପିତ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ ।
(i) CuSO4 + Zn → ZnSO4 + Cu (କପର ସଲ୍ଫେଟ୍ + ଦସ୍ତା → ଦସ୍ତା ସଲ୍ଫେଟ୍ + କପର)
ଏହି ପ୍ରତିକ୍ରିୟାରେ Zn ଖଣ୍ଡର କିଛି ଅଂଶ CuSO4 ଯୌଗିକର Cuକୁ ବିସ୍ଥାପିତ କରି ତାହାର ସ୍ଥାନ ଅଧିକାର କରେ, ଯଦ୍ବାରା CuSO4 ଓ Cu ସୃଷ୍ଟି ହୁଏ । ଏହି ପ୍ରତିକ୍ରିୟାକୁ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା (Displacement Reaction) କୁହାଯାଏ । ଏଥିରେ ଥିବା ଦ୍ରବଣର ନୀଳରଙ୍ଗ ଈଷତ୍ ସବୁଜ ରଙ୍ଗ ହୋଇଯାଏ ।
(ii) ଲୁହା ଧାତୁ କପର ସଲ୍ଫେଟ୍ ଦ୍ରବଣରୁ ତମ୍ବା ଧାତୁକୁ ବିସ୍ଥାପିତ କରେ ।
CuSO4 + Fe → FeSO4 + Cu (କପର ସଲ୍ଫେଟ୍ + ଲୁହା → ଲୌହ ସଲ୍ଫେଟ୍ + କପର)
ଏହି ପ୍ରତିକ୍ରିୟାରେ Fe, CuSO4 ଯୌଗିକର Cuକୁ ବିସ୍ଥାପିତ କରି ତାହାର ସ୍ଥାନ ଅଧିକାର କରେ, ଯଦ୍ବାରା 4 ଓ Cu ସୃଷ୍ଟି ହୁଏ । ଏହି ପ୍ରତିକ୍ରିୟା ମଧ୍ୟ ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟାର ଉଦାହରଣ ଅଟେ ।
(iii) FeSO + Zn → ZnSO4 + Fe
ଈଷତ୍ ସବୁଜ ରଙ୍ଗର ଦ୍ରବଣ
ଏହି ପ୍ରତିକ୍ରିୟାରେ Zn, FeSO4 ଯୌଗିକର Fe କୁ ବିସ୍ଥାପିତ କରି ତାହାର ସ୍ଥାନ ଅଧୁକାର କରେ, ଯଦ୍ବାରା ZnSO4 ଓ Fe ସୃଷ୍ଟି ହୁଏ । ଏହି ପ୍ରତିକ୍ରିୟା ମଧ୍ୟ ‘ବିସ୍ଥାପନ ପ୍ରତିକ୍ରିୟା’ର ଆଉ ଏକ ଉଦାହରଣ ଅଟେ । ଏଥିରେ ଥିବା ଦ୍ରବଣର ଈଷତ୍ ସବୁଜ ରଙ୍ଗ ବଣ୍ଟିହୀନ ହୋଇଯାଏ ଏବଂ ଏଥିରେ ପକାଯାଇଥିବା Zn ଖଣ୍ଡ ଉପରେ ଧଳା ରଙ୍ଗର ଆବରଣ ଦେଖାଯାଏ । ଅଧିକ କ୍ରିୟାଶୀଳ ଧାତୁ କମ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁର ଲବଣର ଦ୍ରବଣରୁ ସେହି ଧାତୁକୁ ବିସ୍ଥାପିତ କରି ନିଜେ, ସେହି ସ୍ଥାନ ଅଧୁକାର କରେ; ଯାହାଫଳରେ ନୂତନ ଲବଣ ଓ ନୂତନ ଧାତୁ ସୃଷ୍ଟି ହୁଏ । ଅଧାତୁ ଓ ଲବଣ ମଧ୍ଯରେ ସାଧାରଣତଃ ପ୍ରତିକ୍ରିୟା ସଂଘଟିତ ହୁଏ ନାହିଁ ।
→ ଧାତୁ ଓ ଅଧାତୁଗୁଡ଼ିକର ଉପଯୋଗିତା (Uses of Metals and Non-metals) :
(i) ଉଭୟ ପ୍ରାଣୀ ଶରୀର ଓ ଉଭିଦ ଶରୀର ଅନେକ ଧାତୁ ଓ ଅଧାତୁର ଯୌଗିକରେ ଗଢ଼ା ହୋଇଛି ।
(ii) ବଞ୍ଚିରହିବାପାଇଁ ସୋଡ଼ିୟମ୍, ପୋଟାସିୟମ୍, କାଲସିୟମ୍, ଆଇରନ୍, କପର, ଜିଙ୍କ୍ ଆଦି ଧାତୁ ଏବଂ ହାଇଡ୍ରୋଜେନ୍, ନାଇଟ୍ରୋଜେନ୍, ଅକ୍ସିଜେନ୍, କାର୍ବନ, ଫସ୍ଫରସ୍, ସଲ୍ଫର୍, ଆୟୋଡିନ୍ ଆଦି ଅଧାତୁ
(iii) ଶ୍ଵାସକ୍ରିୟା ଓ ଦହନ ପାଇଁ ଅକ୍ସିଜେନ୍ ଆବଶ୍ୟକ ।
(iv) ଜଳ, ହାଇଡ୍ରୋଜେନ୍ ଓ ଅକ୍ସିଜେନ୍ର ଯୌଗିକ ଅଟେ ।
(v) ସବୁଜ ଉଭିଦ ବାୟୁରୁ କାର୍ବନ ଡାଇଅକ୍ସାଇଡ୍ (ଅଙ୍ଗାରକାମ୍ଳ) ଓ ମୃତ୍ତିକାରୁ ଜଳ ଅବଶୋଷଣ କରି ସଂଶ୍ଳେଷଣ ପ୍ରକ୍ରିୟାଦ୍ଵାରା ଶ୍ଵେତସାର ଖାଦ୍ୟ ପ୍ରସ୍ତୁତ କରିଥାଏ । ଏହା କେତେକ ଜୀବଙ୍କର ପ୍ରତ୍ୟକ୍ଷ ଖାଦ୍ୟ ଅଟେ ଏବଂ ଅବଶିଷ୍ଟ ଜୀବଙ୍କର ପରୋକ୍ଷ ଖାଦ୍ୟ ଅଟେ ।
(vi) ଆମର ସମସ୍ତ ଖାଦ୍ୟ ଶ୍ଵେତସାର, ପୁଷ୍ଟିସାର, ସ୍ନେହସାର, ଧାତୁସାର, ଭିଟାମିନ୍ ଓ ଜଳ – ଏସବୁ ଧାତୁ ଓ ଅଧାତୁରେ ତିଆରି ପଦାର୍ଥ ।
(vii) ପ୍ରକୃତିରୁ ଉପଲବ୍ଧ ଔଷଧ, ତନ୍ତୁ, ରବର, ଅଠା, ଜୀବାଶ୍ମ ଇନ୍ଧନ ଆଦି ଧାତୁ ଓ ଅଧାତୁରୁ ପ୍ରସ୍ତୁତ ହୁଏ । ମନୁଷ୍ୟକୃତ ଔଷଧ, କୀଟନାଶକ ଔଷଧ, ରାସାୟନିକ ସାର, କୃତ୍ରିମ ତନ୍ତୁ, ପ୍ଲାଷ୍ଟିକ ଆଦି ମଧ୍ଯ ଧାତୁ ଓ ଅଧାତୁରୁ , ସୃଷ୍ଟି ହୋଇଥାଏ ।
(viii) କଳକାରଖାନା, ଇଞ୍ଜିନ୍ ଇତ୍ୟାଦିରେ ବ୍ୟବହୃତ ଯନ୍ତ୍ରପାତି, ଅଟୋମୋବାଇଲ୍, ଉଡ଼ାଜାହାଜ, ଟ୍ରେନ୍, କୃତ୍ରିମ ଉପଗ୍ରହ ଇତ୍ୟାଦିର ଅଂଶ ତିଆରି କରିବାରେ ତଥା ବିଭିନ୍ନ ଘରକରଣା ଜିନିଷ ରନ୍ଧନ ପାତ୍ର, ବାସନକୁସନ,


ବିଷୟଭିତ୍ତିକ ଶବ୍ଦାବଳୀ :