Odisha State Board BSE Odisha 9th Class Physical Science Solutions Chapter 3 ପରମାଣୁ ଓ ଅଣୁ Textbook Exercise Questions and Answers.
BSE Odisha Class 9 Physical Science Solutions Chapter 3 ପରମାଣୁ ଓ ଅଣୁ
1. ରାସାୟନିକ ସଂଯୋଗର ଦୁଇଟି ନିୟମ ଲେଖ ଏବଂ ରୁଟାଅ |
ଉ-
ରାସାୟନିକ ସଂଯୋଗର ଦୁଇଟି ନିୟମ ହେଲା- ବସ୍ତୁତ୍ଵ ସଂରକ୍ଷଣ ନିୟମ ଓ ସ୍ଥିରାନୁପାତ ନିୟମ ।
ବସ୍ତୁତ୍ଵ ସଂରକ୍ଷଣ ନିୟମ :
- ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ବସ୍ତୁତ୍ଵର ସୃଷ୍ଟି ନାହିଁ କିମ୍ବା ବିନାଶ ନାହିଁ ।
- ଯେତେବେଳେ ଏକ ରାସାୟନିକ ପରିବର୍ତ୍ତନ ବା ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟେ, ସେତେବେଳେ ବସ୍ତୁତ୍ଵର ପରିବର୍ତ୍ତନ ଘଟିନଥାଏ । ଅର୍ଥାତ୍ ପରିବର୍ତ୍ତନର ପୂର୍ବ-ବସ୍ତୁତ୍ଵ ଓ ପର-ବସ୍ତୁତ୍ଵ ସମାନ ରହିଥାଏ ।
ଉଦାହରଣ – 2 ଗ୍ରାମ୍ ଉଦ୍ଜାନ 71 ଗ୍ରାମ୍ କ୍ଲୋରିନ୍ ସହ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା କଲେ 73 ଗ୍ରାମ୍ ହାଇଡ୍ରୋଜେନ୍ କ୍ଲୋରାଇଡ୍ ଉତ୍ପନ୍ନ ହୁଏ ।
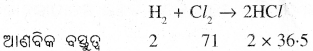
ଉପରୋକ୍ତ ସମୀକରଣରୁ ସ୍ପଷ୍ଟ ହୁଏ ଯେ ପ୍ରତିକାରକଗୁଡ଼ିକର ମୋଟ ବସ୍ତୁତ୍ୱ ଉତ୍ପାଦଗୁଡ଼ିକର ମୋଟ ବସ୍ତୁତ୍ଵ ସହ ସମାନ |
ସ୍ଥିରାନୁପାତ ନିୟମ :
- ରାସାୟନିକ ଯୌଗିକରେ ମୌଳିକଗୁଡ଼ିକ ସର୍ବଦା ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ବସ୍ତୁତ୍ଵ ଅନୁପାତରେ ରହିଥାଏ ।
- କୌଣସି ଏକ ଯୌଗିକ ପଦାର୍ଥ ଯେପରି ପ୍ରସ୍ତୁତ ହେଉ ନା କାହିଁକି କିମ୍ବା ଯେକୌଣସି ଉତ୍ସରୁ ମିଳିଥାଉ, ସେଥୁରେ ସମାନ ମୌଳିକଗୁଡ଼ିକ ସର୍ବଦା ଏକ ନିର୍ଦ୍ଦିଷ୍ଟ ବସ୍ତୁତ୍ଵ ଅନୁପାତରେ ସଂଯୁକ୍ତ ହେବାଦ୍ଵାରା ତାହା ସୃଷ୍ଟି ହୋଇଥାଏ ।
ଉଦାହରଣ :
- ଜଳକୁ ଯେକୌଣସି ଉତ୍ସରୁ ସଂଗ୍ରହ କଲେ ମଧ୍ୟ ଜଳରେ ସର୍ବଦା ହାଇଡ୍ରୋଜେନ୍ ଓ ଅକ୍ସିଜେନ୍ 1: 8 ବସ୍ତୁତ୍ୱ ଅନୁ ପାତରେ ସଂଯୁକ୍ତ ହୋଇଥାଏ । ୨ ଗ୍ରାମ୍ ଜଳକୁ ବିଘଟନ କଲେ ସର୍ବଦା । ଗ୍ରାମ୍ ହାଇଡ୍ରୋଜେନ୍ ଏବଂ ୫ ଗ୍ରାମ୍ ଅକ୍ସିଜେନ୍ ମିଳିଥାଏ ।
- କାର୍ବନ ଡାଇଅକ୍ସାଇଡ଼କୁ ଯେକୌଣସି ପ୍ରଣାଳୀରେ ପ୍ରସ୍ତୁତ କରାଯାଉ କିମ୍ବା ଯେକୌଣସି ଉତ୍ସରୁ ସଂଗ୍ରହ କରାଯାଉ, ସେଥ୍ରେ କାର୍ବନ ଓ ଅକ୍ସିଜେନ୍ର ବସ୍ତୁତ୍ଵର ଅନୁପାତ ସର୍ବଦା 3 : 8 ହେବ ।
2. ଡାଲ୍ନ୍ଙ୍କ ପରମାଣୁ ତତ୍ତ୍ଵର ସ୍ଵୀକାରଗୁଡ଼ିକ ଲେଖ ।
ଉ –
ଡାଲ୍ନ୍ଙ୍କ ପରମାଣୁ ତତ୍ତ୍ବ : ବୈଜ୍ଞାନିକ ଜନ୍ ଡାଲ୍ଟନ୍ 1808 ମସିହାରେ ପଦାର୍ଥର ଗଠନ ସଂପର୍କରେ ଏକ ନୂତନ ତତ୍ତ୍ଵ ଉପସ୍ଥାପନ କରିଥିଲେ । ଏହାକୁ ଡାଲ୍ଟନ୍ ଙ୍କ ପରମାଣୁ ତତ୍ତ୍ୱ କୁହାଯାଏ । ଏହି ତତ୍ତ୍ଵର ସ୍ଵୀକାରଗୁଡ଼ିକ
ହେଲା –
- ପଦାର୍ଥ ଅନେକଗୁଡ଼ିଏ ଅତି କ୍ଷୁଦ୍ର କଣିକାଦ୍ଵାରା ଗଠିତ । ସେହି କଣିକାକୁ ପରମାଣୁ କୁହାଯାଏ ।
- ପରମାଣୁଗୁଡ଼ିକ ଅବିଭାଜ୍ୟ କଣିକା, ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାରେ ଏହାକୁ ସୃଷ୍ଟି କରାଯାଇପାରିବ ନାହିଁ କିମ୍ବା ବିନାଶ କରାଯାଇପାରିବ ନାହିଁ ।
- କୌଣସି ଏକ ମୌଳିକର ପରିମାଣୁଗୁଡ଼ିକର ବସ୍ତୁତ୍ଵ ଓ ରାସାୟନିକ ଧର୍ମ ସମାନ ।
- ବିଭିନ୍ନ ମୌଳିକର ପରମାଣୁଗୁଡ଼ିକର ବସ୍ତୁତ୍ଵ ଓ ରାସାୟନିକ ଧର୍ମ ଭିନ୍ନ ହୋଇଥାଏ ।
- ଛୋଟ ପୂର୍ଣ୍ଣସଂଖ୍ୟା ଅନୁପାତରେ ବିଭିନ୍ନ ମୌଳିକର ପରମାଣୁଗୁଡ଼ିକ ସଂଯୁକ୍ତ ହୋଇ ଯୌଗିକ ସୃଷ୍ଟି ହୋଇଥାଏ ।
3. ଗୋଟିଏ ଉଦାହରଣ ସହ ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ କ’ଣ ବୁଝାଅ ।
ଉ –
ପାରମାଣବିକ ବସ୍ତୁତ୍ୱ ଏକକରେ ମୌଳିକର ପରମାଣୁର ହାରାହାରି ବସ୍ତୁତ୍ଵ ହେଉଛି ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ |
ଉଦାହରଣ : ପ୍ରକୃତିରେ ଉପଲବ୍ଧ ଅକ୍ସିଜେନ୍ର ଆଇସୋଟୋପ୍ଗୁଡିକ ହେଲା- 160, 170 ଓ 180 1 ସେଗୁଡିକର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ ଯଥାକ୍ରମେ 15.995 u, 16.999 u ଓ 17.999 u । ଏହି ଆଇସୋଟୋପ୍ଗୁଡିକର ଆପେକ୍ଷିକ ପରିମାଣ ଯଥାକ୍ରମେ 99.763%, 0.037% ଓ 0.200% |
∴ ଅମ୍ଳଜାନର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ = ![]()
= 15.999u = 16u |
![]()
4. ଆଣବିକ ବସ୍ତୁତ୍ଵ କ’ଣ ? ଏକ ଯୌଗିକର ଆଣବିକ ବସ୍ତୁତ୍ୱ କିପରି ନିର୍ଣ୍ଣୟ କରାଯାଇପାରିବ, ଉଦାହରଣ ଦେଇ ଲେଖ ।
ଉ –
ଆଣବିକ ବସ୍ତୁତ୍ଵ : ଆଣବିକ ବସ୍ତୁତ୍ଵ ହେଉଛି, ଗୋଟିଏ ଅଣୁରେ ଥିବା ସମସ୍ତ ପରମାଣୁର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵର ଯୋଗଫଳ । ଆଣବିକ ବସ୍ତୁତ୍ଵ ଏକ ଆନୁପାତିକ ସଂଖ୍ୟା ଏବଂ ଏହାର ଏକକ u ।
ଉଦାହରଣ :
କାର୍ବନ ଡାଇଅକ୍ସାଇଡ୍ର ଆଣବିକ ବସ୍ତୁତ୍ଵ ନିର୍ଣ୍ଣୟ :
କାର୍ବନ ଡାଇଅକ୍ସାଇଡ୍ର ସଂକେତ = CO2
କାର୍ବନର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ = 12u,
ଅକ୍ସିଜେନ୍ର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ କାର୍ବନ ଡାଇଅକ୍ସାଇଡ଼ର ଆଣବିକ ବସ୍ତୁତ୍ଵ = 16u
∴ କାର୍ବନ ଡାଇଅକ୍ସାଇଡ୍ର ଆଣବିକ ବସ୍ତୁତ୍ଵ
= 1 x କାର୍ବନର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ + 2 x ଅକ୍ସିଜେନ୍ର ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ
= 1 × 12u + 2 × 16u = 12u + 32 u = 44u
5. ପଲିଆଟମିକ୍ ଆୟନ କ’ଣ ? ଚାରୋଟି ପଲିଆଟମିକ୍ ଆୟନର ଉଦାହରଣ ଦିଅ ।
ଉ –
ପଲିଆଟମିକ୍ ଆୟନ : ଗୋଟିଏ ଚାର୍ଜଯୁକ୍ତ ପରମାଣୁରେ ଆୟନ ଗଠିତ ହୋଇପାରେ କିମ୍ବା ଏକାଧ୍ଵ ପରମାଣୁ ଏକତ୍ର ହୋଇ ଯୁକ୍ତ ବା ବିଯୁକ୍ତ ଚାର୍ଜ ବହନ କରିପାରେ । ଏକାଧିକ ପରମାଣୁ ଏକତ୍ର ହୋଇ ଚାର୍ଜ ବହନ କରିଥିଲେ ସେଗୁଡ଼ିକୁ ପଲିଆଟମିକ୍ ଆୟନ କୁହାଯାଏ ।
ଉଦାହରଣ –

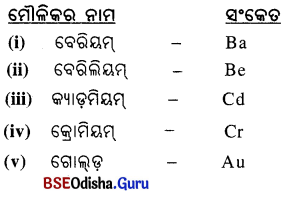
6. ନିମ୍ନଲିଖୁତ ମୌଳିକଗୁଡ଼ିକର ପ୍ରତୀକ ଲେଖ ।
(i) ବେରିୟମ୍
(ii) ବେରିଲିୟମ୍
(iii) କ୍ୟାଡ୍ମିୟମ୍
(iv) କ୍ରୋମିୟମ୍
(v) ଗୋଲ୍ଡ
ଉ –
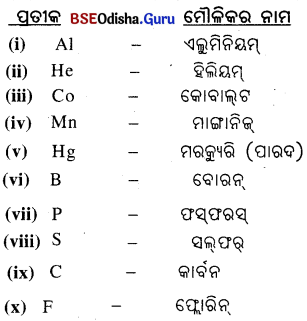
7. ନିମ୍ନଲିଖୁତ ପ୍ରତୀକଗୁଡ଼ିକରୁ ମୌଳିକର ନାମ ଲେଖ ।
(i) Al
(ii) He
(iii) Co
(iv) Mn
(v) Hg
(vi) B
(vii) P
(viii) S
(ix) C
(x) F
ଉ –
8. ରାସାୟନିକ ସଂକେତ ଲେଖୁବାର ପ୍ରଣାଳୀ ବୁଝାଅ ।
ଉ –
ରାସାୟନିକ ସଂକେତ ଲେଖୁବାର ପ୍ରଣାଳୀ : ରାସାୟନିକ ସଂକେତ ଲେଖୁବେଳେ ନିମ୍ନଲିଖ୍ତ ନିୟମମାନ ଅବଲମ୍ବନ କରାଯାଏ ।
- କୌଣସି ଯୌଗିକର ଅଣୁର ଆଣବିକ ବା ରାସାୟନିକ ସଂକେତ ଲେଖିବାକୁ ହେଲେ ପ୍ରଥମେ ଏଥିରେ ଥିବା ମୌଳିକଗୁଡ଼ିକର ପ୍ରତୀକକୁ ପାଖାପାଖୁ ଲେଖାଯାଏ ।
- ଧାତୁ ଏବଂ ଅଧାତୁରୁ ଗଠିତ ଯୌଗିକ ପାଇଁ ଧାତୁର ନାମ କିମ୍ବା ପ୍ରତୀକ ପ୍ରଥମେ ଲେଖାଯାଏ ।
ଉଦାହରଣ – ମ୍ୟାଗ୍ନେସିୟମ୍ ଅକ୍ସାଇଡ୍ (MgO), ପୋଟାସିୟମ୍ ବ୍ରୋମାଇଡ୍ (KBr) । - ମୌଳିକଗୁଡ଼ିକର ଯୋଗ୍ୟତା ପ୍ରତୀକର ଠିକ୍ ତଳେ ଲେଖାଯାଏ ।
- ତା’ପରେ ଯୋଗ୍ୟତା ସଂଖ୍ୟା ଦୁଇଟିର ସ୍ଥାନ ଅଦଳବଦଳ କରି ସଙ୍କେତ ଲେଖାଯାଏ ।
- ଆୟନର ଯୋଗ୍ଯତା କିମ୍ବା ଚାର୍ଜ ସମତୁଲ ହେବ ।
- ପଲିଆଟମିକ୍ ଆୟନରୁ ସୃଷ୍ଟ ଯୌଗିକରେ ଆୟନକୁ ବନ୍ଧନୀ ମଧ୍ଯରେ ରଖ୍ ଅନୁ ପାତ ସୂଚାଉଥିବା ସଂଖ୍ୟାଟି ଲେଖାଯାଏ । ଏହି ସଂଖ୍ୟା ଯଦି ଏକ ହୋଇଥାଏ, ବନ୍ଧନୀର ଆବଶ୍ୟକତା ନାହିଁ ।
ଉଦାହରଣ – HNO3
ଉଦାହରଣ

![]()
9. ନିମ୍ନଲିଖୁ ଯୌଗିକମାନଙ୍କର ସଙ୍କେତ ଲେଖ ।
(i) ସୋଡ଼ିୟମ୍ କ୍ରୋମାଇଡ୍
(ii) ଜିଙ୍କ୍ ସଲଫେଟ୍
(iii) ଏମୋନିୟମ୍ କ୍ଲୋରାଇଡ୍
(iv) ବେରିୟମ୍ କାର୍ବୋନେଟ୍
(v) ଏଲୁମିନିୟମ୍ ଫସ୍ଫେଟ୍
ଉ –

10. ପାଞ୍ଚୋଟି ଅଧାତୁର ନାମ ଲେଖୁ ସେଗୁଡ଼ିକର ପରମାଣୁକତା ଲେଖ ।
ଉ –

11. ଏଭୋଗାଡ୍ରୋ ସ୍ଥିରାଙ୍କ କ’ଣ ବୁଝାଅ ।
ଉ
ଏଭୋଗାଡ୍ରୋ ସ୍ଥିରାଙ୍କ :
(i) ଏକ ମୋଲ୍ କହିଲେ 6.02 x 1023 ସଂଖ୍ୟାକୁ ବୁଝାଏ । ଏହି ବିରାଟ ସଂଖ୍ୟାକୁ ଏଭୋଗାଡ୍ରୋ ସ୍ଥିରାଙ୍କ ବା ଏଭୋଗାଡ୍ରୋ ସଂଖ୍ୟା କୁହାଯାଏ । ଏହାକୁ N0 ପ୍ରତୀକଦ୍ଵାରା ଚିହ୍ନିତ କରାଯାଏ ।
1 N0 = 6.02 x 1023 ସଂଖ୍ୟାକ କଣିକା |
(ii) ଏହା ଅଣୁ, ପରମାଣୁ, ଆୟନ ବା କଣିକା ସଂଖ୍ୟା ଗଣନାର ଗୋଟିଏ ଏକକ ।
ଉଦାହରଣ –
1 ମୋଲ୍ ହାଇଡ୍ରୋଜେନ୍ ପରମାଣୁ = 6:02 x 1023 ସଂଖ୍ୟକ ହାଇଡ୍ରୋଜେନ୍ ପରମାଣୁ
1 ମୋଲ୍ କ୍ଲୋରିନ୍ ଅଣୁ = 6:02 x 1023 ସଂଖ୍ୟକ କ୍ଲୋରିନ୍ ଅଣୁ ।
1 ମୋଲ୍ ଆୟନ = 6-02 x 1023 ସଂଖ୍ୟକ ଆୟନ ।
1 ମୋଲ୍ ଇଲେକ୍ଟ୍ରନ୍ = 6.02 × 1023 ସଂଖ୍ୟକ ଇଲେକ୍ଟ୍ରନ୍ |
12. ଗ୍ରାମ୍ -ଆଣବିକ ବସ୍ତୁତ୍ଵ କ’ଣ ଗୋଟିଏ ଉଦାହରଣ ସହ ବୁଝାଅ ।
ଉ-
ଗ୍ରାମ୍-ଆଣବିକ ବସ୍ତୁତ୍ଵ : ଏକ ମୋଲ୍ ପଦାର୍ଥର ବସ୍ତୁତ୍ଵକୁ ‘ମୋଲାର ବସ୍ତୁତ୍ଵ’ କୁହାଯାଏ । ପରମାଣୁର
ମୋଲାର ବସ୍ତୁତ୍ଵକୁ ଗ୍ରାମ୍-ପାରମାଣବିକ ବସ୍ତୁତ୍ଵ ଏବଂ ଅଣୁର ମୋଲାର ବସ୍ତୁତ୍ଵକୁ ଗ୍ରାମ-ଆଣବିକ ବସ୍ତୁତ୍ଵ କୁହାଯାଏ ।
ଉଦାହରଣ –
- ହାଇଡ୍ରୋଜେନ୍ର ଆଣବିକ ବସ୍ତୁତ୍ଵ = 2u
- ଏକ ମୋଲ୍ ହାଇଡ୍ରୋଜେନ୍ ଅଣୁ (H2)ର ବସ୍ତୁତ୍ଵ = 2 ଗ୍ରାମ୍
- ହାଇଡ୍ରୋଜେନ୍ର ଗ୍ରାମ୍-ଆଣବିକ ବସ୍ତୁତ୍ଵ = 2 ଗ୍ରାମ୍
- ସେହିପରି ଜଳର ଆଣବିକ ବସ୍ତୁତ୍ଵ = 18 u
- ଜଳର ଗ୍ରାମ୍ ଆଣବିକ ବସ୍ତୁତ୍ଵ = 18 ଗ୍ରାମ୍
- 18 ଗ୍ରାମ୍ ଜଳରେ 1 ମୋଲ୍ ଜଳ ଅଣୁ ଅର୍ଥାତ୍ 6.02 x 1023 ସଂଖ୍ୟକ ଜଳ ଅଣୁ ରହିଛି ।
କାର୍ଯ୍ୟାବଳୀ (Activity)
ତୁମପାଇଁ କାମ 3.1 :
ପରୀକ୍ଷା : ଗୋଟିଏ କୋନିକାଲ ଫ୍ଲାସ୍କରେ 10 ml ସୋଡ଼ିୟମ ସଲ୍ଫେଟ୍ର5% ଦ୍ରବଣ ଓ ଏକ ଜ୍ଵଳନ ‘ନଳୀରେ 10ml ବେରିୟମ କ୍ଲୋରାଇଡ଼ର 5% ଦ୍ରବଣ ନିଆଯାଉ । କୋନିକାଲ୍ ଫ୍ଲସ୍କ ଭିତରେ ଯତ୍ନର ସହିତ ଜ୍ଵଳନ ନଳୀଟି ଝୁଲାଯାଉ, ଯେପରି ଦ୍ରବଣଗୁଡ଼ିକ ମିଶି ନ ଯାଆନ୍ତି । ଫ୍ଲସ୍କ ମୁହଁରେ ଏକ କର୍କ ଠିପି ଲଗାଯାଉ । ବର୍ତ୍ତମାନ କୋନିକାଲ୍ ଫ୍ଲସ୍କର ଓଜନ ନିଆଯାଉ । ଫ୍ଲାସ୍କଟିକୁ ଟିକେ ଅଣେଇ ଦିଆଯାଉ, ଯେପରି ଦୁଇଟିଯାକ ଦ୍ରବଣ ମିଶିଯିବ । ଫ୍ଲସ୍କର ତଳପଟକୁ ଆସ୍ତେ ଆସ୍ତେ ହଲାଇଲେ ବ୍ରଦଣଦ୍ୱୟ ଭଳଭାବରେ ମିଶିଯିବ |
ପର୍ଯ୍ୟବେକ୍ଷଣ : ଫ୍ଲସ୍କରେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟା ଘଟି ଧଳାରଙ୍ଗର ସଲ୍ଫେଟ୍ ଅବକ୍ଷେପ (Precipitate) ସୃଷ୍ଟି ହେବ । ବର୍ତ୍ତମାନ ପୁଣିଥରେ ଫ୍ଲାସ୍କକୁ ଓଜନ କରାଯାଉ । ଓଜନରୁ ଜଣାଯିବ ଯେ ଓଜନଦ୍ଵୟ ମଧ୍ଯରେ କିଛି ପାର୍ଥକ୍ୟ ନାହିଁ |
ସିଦ୍ଧାନ୍ତ : ଏଥୁରୁ ଜଣାଗଲା ଯେ ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାଦ୍ଵାରା ବସ୍ତୁତ୍ଵର କିଛି ପରିବର୍ତ୍ତନ ହୁଏ ନାହିଁ ।

ତୁମପାଇଁ କାମ 3.2 :
ତଳେ କେତେକ ମୌଳିକ ପରମାଣୁର ମଡ଼େଲ ଚିତ୍ର ଦିଆଯାଇଛି ।
![]()
ଏହି ଚିତ୍ରଗୁଡ଼ିକ ବ୍ୟବହାର କରି ଭିନ୍ନ ଭିନ୍ନ ଅଣୁର ମଡ଼େଲ ଚିତ୍ର ଅଙ୍କନ କର ।
![]()
ଏହି ପଦ୍ଧତି ଅବଲମ୍ବନ କରି ତଳେ ଦିଆଯାଇଥିବା ଅଣୁଗୁଡ଼ିକର ମଡ଼େଲ ଚିତ୍ର ଅଙ୍କନ କର ।
CO2, NO2, N2, SO2, SO3, NH3, O2, CH4, CS2, H2O
ଉ –